Đông cứng dáng đi trong bệnh Parkinson: tần suất, đặc điểm lâm sàng, các yếu tố nguy cơ và điều trị hiện nay
Đông cứng dáng đi trong bệnh Parkinson: Tần suất, đặc điểm lâm sàng, các yếu tố nguy cơ và điều trị hiện nay
Lê Thành Nhân1, Trần Ngọc Tài2
Bộ môn Thần kinh, Đại học Y Dược TP. Hồ Chí Minh1
Đơn vị Rối loạn vận động, Khoa Thần kinh, Bệnh viện Đại học Y Dược, Đại học Y Dược TP. Hồ Chí Minh2
Tóm tắt
Bệnh Parkinson là bệnh lý thoái hóa thần kinh tiến triển này càng nặng dần được đặc trưng bởi các triệu chứng vận động và ngoài vận động. Ngoài các triệu chứng vận động điển hình, người bệnh Parkinson còn có một dáng đi đặc trưng gọi là đông cứng dáng đi (freezing of gait). Tần suất đông cứng dáng đi ở người bệnh Parkinson dao động từ 14% đến 55,1%. Triệu chứng này dẫn đến tăng nguy cơ té ngã ở người bệnh Parkinson, tăng sự phụ thuộc, giảm khả năng tự đi lại và ảnh hưởng nặng đến chất lượng cuộc sống người bệnh. Đông cứng dáng đi được xác định bằng phương pháp chủ quan qua hỏi bệnh hoặc bảng câu hỏi, hoặc được xác định khách quan thông qua khám lâm sàng hoặc phân tích video. Các phương pháp điều trị chính cho đông cứng dáng đi gồm vật lý trị liệu, thuốc và phẫu thuật.
Mở đầu
Bệnh Parkinson là bệnh lý thoái hóa thần kính tiến triển này càng nặng dần có tỉ lệ cao thứ hai chỉ sau bệnh Alzeimer [1]. Bệnh được đặc trưng bởi các triệu chứng vận động và ngoài vận động. Những triệu chứng vận động chính ở người bệnh Parkinson bao gồm chậm vận động, đơ cứng, run khi nghỉ và mất ổn định tư thế [2]. Cùng với các triệu chứng trên, người bệnh Parkinson còn có các bất thường dáng đi, thấy được trong quá trình bệnh diễn tiến bệnh [3]. Dáng đi điển hình là dáng đi chậm, giảm đong đưa tay, bước chân nhỏ hơn, mất ổn định tư thế và mất phối hợp vận động tay và thân mình khi đi[4]. Ngoài dáng đi điển hình trên, người bệnh Parkinson còn có một dáng đi đặc trưng khác gọi là đông cứng dáng đi [3].
Đông cứng dáng đi được định nghĩa là một cơn ngắn, xảy ra từng lúc mà trong cơn có sự biến mất hoặc giảm rõ rệt sự tiến về phía trước của bàn chân dù bệnh nhân mong muốn đi tới[5]. Người bệnh đột ngột cảm thấy bàn chân họ như dính vào sàn nhà khi cố gắng bước tới. Thông thường, đông cứng kéo dài vài giây, tuy nhiên nó có thể kéo dài hơn 30 giây hoặc thậm chí vài phút, đôi khi khiến người bệnh hoàn toàn không thể bước tới được nếu không có hỗ trợ [6]. Triệu chứng này dẫn đến tăng nguy cơ té ngã ở người bệnh Parkinson, tăng sự phụ thuộc, giảm khả năng tự đi lại và ảnh hưởng nặng đến chất lượng cuộc sống người bệnh [7, 8].
Đông cứng dáng đi được xem là một triệu chứng của bệnh Parkinson cũng như của hội chứng Parkinson do nhiều nguyên nhân khác nhau [9]. Trong bệnh Parkinson, đông cứng dáng đi được xem là triệu chứng muộn. Tuy nhiên, những nghiên cứu gần đây cho thấy đông cứng dáng đi có thể xảy ra ở giai đoạn rất sớm của bệnh Parkinson [5].
Tần suất đông cứng dáng đi
Tần suất của đông cứng dáng đi trong nhóm bệnh nhân Parkinson thì thay đổi giữa các nghiên cứu, dao động từ 14% đến 55,1% [10, 11]. Đông cứng dáng đi có thể xuất hiện ở bất kỳ giai đoạn nào của bệnh, nhưng thường gặp nhất ở giai đoạn muộn của bệnh, có thể lên đến 83% [12].
Sự khác biệt về tần suất này do nhiều yếu tố khác nhau. Các yếu tố có thể bao gồm cách triệu chứng này được chẩn đoán, bản chất của người bệnh Parkinson được nghiên cứu, thời gian nghiên cứu, chất lượng của nghiên cứu cũng như các yếu tố về địa lý, chủng tộc [13],[14].
Sinh lý bệnh đông cứng dáng đi
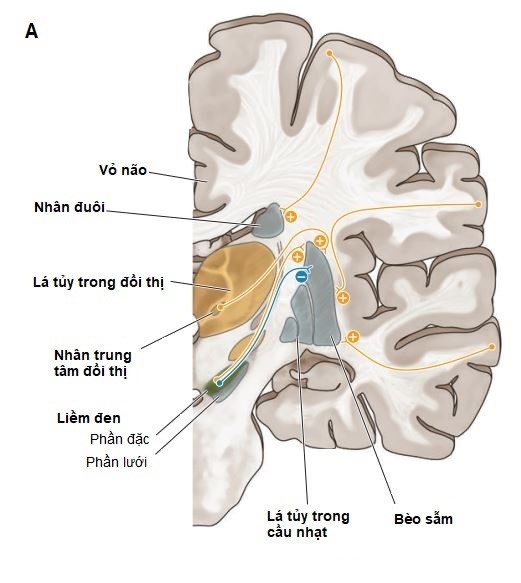
Để đi lại bình thường, tất cả các hệ thống và chức năng sau phải toàn vẹn gồm chức năng vận động (cho khởi đầu đi và duy trì bước đi theo nhịp), thăng bằng, phản xạ tư thế, chức năng cảm giác, phối hợp vận động cảm giác, kiểm soát vận động, hệ cơ xương và chức năng tim phổi. Hệ thống kết hợp trung ương bao gồm vỏ não thùy trán, hạch nền, thân não và tiểu não giải mã thông tin nhận cảm và lựa chọn chương trình vận động cần thiết cho sự đi lại[15].
Ở người bệnh Parkinson, suy chức năng của nhiều hệ thống có thể dẫn đến triệu chứng đông cứng dáng đi. Tuy nhiên, sự phức tạp của hệ thần kinh dẫn đến khó xác định vị trí tổn thương thần kinh cụ thể đưa đến đông cứng dáng đi. Cho nên, đã có nhiều cách giải thích về sinh lý bệnh của triệu chứng này, trong đó năm cơ chế sau đây được cho là có thể phù hợp gồm (1) Rối loạn chức năng của trung tâm dáng đi ở tủy sống; (2) Rối loạn kết nối giữa hạch nền với vùng vận động phụ (SMA) và với nhân sâu tiểu não; (3) Sự mất khả năng kết hợp giữa vùng điều hòa tư thế bình thường với mô hình vận động bước; (4) Suy chức năng nhận cảm của não giúp giải thích đông cứng dáng đi xuất hiện khi tiến gần đến khe cửa hẹp; và (5) Rối loạn chức năng điều hành thùy trán, nơi có sự mất kết nối giữa hạch nền và thùy trán, ảnh hưởng đến việc thực hiện nhiều công việc đồng thời [16].
Diễn tiến và các yếu tố liên quan đông cứng dáng đi
Đông cứng dáng đi trong bệnh Parkinson thường xuất hiện ở giai đoạn muộn. Đông cứng dáng đi và dáng đi kiểu chạy chập tới (festinating) có thể xuất hiện và người bệnh tăng nguy cơ té ngã ở giai đoạn này. Nếu đông cứng dáng đi xuất hiện ở giai đoạn sớm của bệnh cần quan tâm đến các nguyên nhân khác, đặc biệt là liệt trên nhân tiến triển. Khi bệnh tiến triển, đông cứng dáng đi trở nên thường xuyên, kết hợp với giảm khả năng thăng bằng và kiểm soát tư thế cũng như nguy cơ té ngã. Dao động vận động và loạn động hiện diện ở hầu hết bệnh nhân và ảnh hưởng xấu đến dáng đi. Khi đông cứng dáng đi trở nên nặng hơn thì người bệnh không tự đi lại được, cần người hỗ trợ hoặc xe lăn [3].
Những yếu tố lâm sàng được xem là yếu tố nguy cơ làm tăng xuất hiện triệu chứng đông cứng dáng đi gồm thời gian bệnh kéo dài, triệu chứng vận động nặng hơn, điểm không run cao hơn hoặc kiểu hình rối loạn dáng đi và mất ổn định tư thế (PIGD), liều levodopa cao hơn, dao động vận động, ảo giác và suy giảm nhận thức [17-21]. Ngoài ra, một số yếu tố về hình ảnh học như tăng tín hiệu chất trắng hay chất chỉ dấu Aβ42 trong dịch não tủy như cũng cho thấy có liên quan đông cứng dáng đi ở người bệnh Parkinson[22].
Các kiểu đông cứng dáng đi
Rối loạn dáng đi thường được chia thành nhóm rối loạn dáng đi liên tục và nhóm rối loạn dáng đi từng đợt. Rối loạn dáng đi liên tục là hậu quả của rối loạn chức năng thần kinh trung ương hoặc ngoại vi mạn tính. Trái lại, những rối loạn dáng đi theo từng đợt không thể đoán trước được. Bệnh nhân không thể thích ứng với những thay đổi nhất thời này và do đó kiểu rối loạn dáng đi này thường là nguyên nhân chính dẫn đến té ngã, lo lắng, sợ hãi và né tránh[23]. Đông cứng dáng đi thuộc nhóm rối loại dáng đi từng đợt này. Có nhiều cách phân loạn đông cứng dáng đi như sau:
Phân loại dựa vào thời điểm xuất hiện: đây là cách phân loại do Fahn và cộng sự đưa ra. Có 5 loại gồm (i) ngập ngừng (hesitation) khi khởi đầu; (ii) ngập ngừng khi xoay người; (iii) ngập ngừng khi đi qua chỗ hẹp; (iv) ngập ngừng khi đến đích; và (v) ngập ngừng trong không gian mở [24].
Phân loại dựa vào kiểu vận động bàn chân: gồm (i) đông cứng thể chập bước: có sự bước tới nhưng với tần số bước tăng nhanh và chiều dài bước chân ngắn lại; (ii) đông cứng thể dậm chân tại chỗ: người bệnh dậm chân tại chỗ với tần số nhanh 2 – 4 Hz nhưng không thể bước tới; và (iii) đông cứng thể đứng yên: không có vận động bàn chân được thấy trong lúc yêu cần bước đi [25].
Phân loại dựa vào sự đáp ứng với thuốc dopaminergic: gồm ba nhóm là (1) đông cứng dáng đi đáp ứng với dopaminergic (còn gọi là đông cứng dáng đi giai đoạn “Tắt”); (2) đông cứng dáng đi không đáp ứng với dopaminergic (còn gọi là đông cứng dáng đi giai đoạn “Bật-Tắt”), và (3) đông cứng dáng đi do thuốc dopaminergic (còn gọi là đông cứng dáng đi giai đoạn “Bật”) [25].
Bảng: Phân loại đông cứng dáng đi theo đáp ứng dopaminergic
| Kiểu đông cứng dáng đi | Giai đoạn “TẮT” | Giai đoạn “BẬT” |
| TẮT | Đông cứng dáng đi xảy ra | Đông cứng dáng đi không xảy ra |
| BẬT | Đông cứng dáng đi không xảy ra | Đông cứng dáng đi xảy ra |
| BẬT-TẮT | Đông cứng dáng đi xảy ra | Đông cứng dáng đi xảy ra |
Khám đông cứng dáng đi
Khám lâm sàng về dáng đi sẽ cung cấp một cái nhìn tổng quan về cấu trúc và chức năng liên quan đến bước đi. Điều quan trọng là phải quan sát toàn bộ bệnh nhân trong khi người bệnh đi bộ trên một khoảng cách ít nhất vài mét. Nếu có thể nên quan sát lúc đối tượng đi chân không.
Có nhiều thách thức trong việc xác định đông cứng dáng đi ở người bệnh Parkinson bao gồm: (1) hiện tượng này xảy ra từng lúc nên không phải lúc nào cũng thấy; (2) đông cứng dáng đi có thể biến mất trong lúc thăm khám do bệnh nhân dành sự chú ý cho dáng đi; và (3) những yếu tố về nhận thức và cảm xúc cũng ảnh hưởng đến sự xuất hiện đông cứng dáng đi. Do đó, phát hiện đông cứng dáng đi cần sự phối hợp phương pháp thăm khám chủ quan và khách quan. Phương pháp chủ quan chủ yếu dựa trên sự nhận thức về triệu chứng của bệnh nhân cũng như người chăm sóc. Những phương pháp khách quan tại phòng khám là cần thiết để xác định đông cứng dáng đi. Chẩn đoán có thể có đông cứng dáng đi (probable freezer) khi đông cứng được xác định bởi hỏi người bệnh hoặc người chăm sóc. Chẩn đoán xác định có đông cứng dáng đi (definite freezer) khi đông cứng dáng đi được quan sát thấy bởi một chuyên gia có kinh nghiệm. Trong thực hành lâm sàng, tiếp cận đông cứng dáng đi phụ thuộc vào tình huống lâm sàng, trong đó phương pháp chủ quan thường được sử dụng nhất, còn phương pháp khách quan thường cần thiết trong các nghiên cứu hoặc khi cần điều chỉnh điều trị. Tuy nhiên, một sự kết hợp cả hai phương pháp này sẽ cho cái nhìn tổng quan hơn về đông cứng dáng đi [26].
Phương pháp chủ quan
Hỏi bệnh sử Hỏi bệnh cho phép sàng lọc đông cứng dáng đi và xác định sự khó chịu do đông cứng dáng đi gây ra. Bệnh nhân có thể được hỏi những trải nghiệm điển hình như cảm giác bàn chân dính trên sàn nhà, hoặc cảm giác không bước tới phía trước hơn là hỏi bệnh nhân có đông cứng hay không. Việc mô tả đông cứng dáng đi là như thế nào cũng rất hữu ích cho cả bệnh nhân và người chăm sóc. Ví dụ: có thể cho bệnh nhân và người chăm sóc xem một video về biểu hiện đông cứng rồi sau đó hỏi lại. Ngoài ra, hỏi thêm về hiệu quả của thuốc là cần thiết để phân loại đông cứng dáng đi đáp ứng hay kháng với dopaminergic. Hơn nữa, đông cứng dáng đi là nguy cơ lớn của té ngã ở người bệnh Parkinson nên rất cần thiết hỏi bệnh nhân về tiền căn té ngã trước đây hoặc nỗi sợ té ngã [27].
Dựa vào bảng câu hỏi Bảng câu hỏi cung cấp một cái nhìn tổng thể về đông cứng dáng đi, có thể được sử dụng trong mục đích nghiên cứu. Điểm MDS-UPDRS phần 2, câu 13 hỏi bệnh nhân về sự hiện diện và độ nặng của đông cứng dáng đi. Tuy nhiên, MDS- UPDRS chỉ cho phép xác định sự hiện diện và gánh nặng của đông cứng dáng đi trong đời sống hằng ngày mà không nêu được những tính chất của nó [28]. Một số thang điểm khác cũng được sử dụng gồm FOGQ[29] và NFOGQ[30]. Thang NFOGQ rất hữu ích để đánh giá độ nặng của đông cứng dáng đi về tần số, cường độ và thời gian kéo dài của cơn đông cứng dài nhất, ảnh hưởng chủ quan lên chất lượng cuộc sống và hoạt động hằng ngày. Tuy nhiên, những câu hỏi chỉ tập trung vào khởi đầu đi và xoay người cũng như những yếu tố kích gợi thường gặp nhất của đông cứng dáng đi những lại không phân biệt giữa đông cứng dáng đi giai đoạn “bật” hay “tắt”.
Phương pháp tiếp cận tại nhà Thực tế đông cứng dáng đi thường xuất hiện nhất khi bệnh nhân ở nhà. Tiếp cận đông cứng dáng đi trong điều kiện tại nhà cho nhiều thông tin hữu ích hơn về hình thái của đông cứng dáng đi xảy ra trong cuộc sống hằng ngày. Một nhật ký đầy đủ sẽ bao gồm số lần đông cứng trong một ngày, thời điểm trong ngày, những tình huống kích gợi (như đi qua một ô cửa), và liệu cơn đông cứng này có gây ra té ngã hay không. Tùy vào mục đích và thời gian, nó cần được theo dõi bởi nhà nghiên cứu hoặc bác sĩ điều trị mỗi tuần để bảo đảm sự hoàn thành một cách chính xác[27]. Tuy nhiên, nhật ký rất khó để ghi lại mức độ đông cứng, đặc biệt đông cứng nặng. Vì hạn chế này, nhật ký nên được kết hợp với những phương pháp tiếp cận khác [26].
Phương pháp khách quan
Tại phòng khám
Điều kiện thuận lợi khi tiếp cận đông cứng dáng đi ở phòng khám là khả năng nhìn thấy và so sánh một bệnh nhân ở cả hai giai đoạn “bật” và “tắt”. Tuy nhiên, trong trường hợp đông cứng giai đoạn “tắt” (loại thường gặp nhất), đặc biệt ở giai đoạn sớm của bệnh Parkinson, đông cứng dáng đi có thể khó phát hiện trong một lần thăm khám bởi vì bệnh nhân thường đã uống thuốc trước khi đến khám. Hơn nữa, điều kiện tại phòng khám khó đánh giá hết độ nặng của đông cứng dáng đi bởi vì thời gian khám quá ngắn để có thể bắt được đông cứng dáng đi và xác định hết các tính chất của nó[26].
MDS-UPDRS phần III mục đông cứng dáng đi cho phép ghi lại thông tin trên lâm sàng về độ nặng của triệu chứng dựa trên những tình huống khởi phát đông cứng dáng đi. Thang điểm này tiếp cận độ nặng của đông cứng dáng đi theo mức độ nặng từ 0 điểm đến 4 điểm. Tuy nhiên, đông cứng chỉ được tiếp cận bởi một mục đơn lẻ, có thể bỏ qua những tình huống kích gợi đông cứng dáng đi khác. Do đó độ nhạy của nó không cao và cũng không đánh giá thời gian kéo dài của cơn đông cứng[28].
Tác giả Ziegler và cộng sự đưa ra một thang điểm lâm sàng đánh giá đông cứng dáng đi, gọi là thang điểm FOG[31]. Thang điểm này đo lường sự xảy ra của đông cứng dáng đi thông qua bốn tình huống có khả năng kích gợi (ngập ngừng khi khởi đầu, xoay theo chiều kim đồng hồ, xoay ngược chiều kim đồng hồ, và trong không gian hẹp) kèm kết hợp hay không kết hợp nhiệm vụ kép (đếm ngược từ 100, bưng khay nước… lúc đi). Tuy nhiên, thang điểm này tiêu tốn nhiều thời gian, lên đến 15 phút để hoàn thành. Hơn nữa, nó không kết hợp tất cả những yếu tố kích gợi của đông cứng dáng đi trong tính toán độ nặng của đông cứng cũng như không xem xét về thời gian kéo dài của cơn đông cứng.
Một số tác giả sử dụng “đạo trình đi” để đánh giá đông cứng dáng đi trong thăm khám lâm sàng[32, 33]. Đặc biệt, hội Bệnh Parkinson và rối loạn vận động thế giới đã đưa ra một đạo trình để hướng dẫn chung về đánh giá dáng đi ở bệnh nhân Parkinson dù tính giá trị chưa được kiểm định[34]. Khám bệnh nhân đông cứng điển hình bao gồm xoay nhanh 360o, đi với bước nhỏ, dừng theo yêu cầu, đi qua chỗ hẹp, thực hiện công việc kép khi đi như cầm một cái mâm, và thực hiện hoạt động nhận thức kép. Việc thăm khám này phải được làm cẩn thận bởi nguy cơ té ngã của bệnh nhân. Những tiếp cận lâm sàng này sẽ được thay đổi tùy từng bệnh nhân. Nếu mục đích đơn giản là xác định đông cứng, tiếp cận sẽ dừng ngay khi triệu chứng xuất hiện. Ngược lại, ở bệnh nhân tự khai có đông cứng dáng đi và không thể xác định được đông cứng khi khám lâm sàng, rất cần thiết sử dụng nhiều yếu tố kích gợi để phát hiện đông cứng dáng đi.
Đôi khi, dù đã sử dụng nhiều yếu tố kích gợi vẫn không gây ra đông cứng dáng đi ở bệnh nhân được gợi ý có đông cứng dáng đi thông qua hỏi bệnh. Trong những trường hợp này, việc đánh giá nên được lặp lại ở những lần thăm khám kế tiếp [26].
Phương pháp tiếp cận tại nhà Hiện tại, nhiều nghiên cứu sử dụng những dụng cụ đeo cảm biến tại nhà để bắt những cơn đông cứng dáng đi. Tuy nhiên, hiện nay các thiết bị này vẫn còn nhiều hạn chế và chưa thể thay thế cho vai trò của các bác sĩ chuyên gia lâm sàng [35, 36].
Điều trị đông cứng dáng đi
Bước đầu tiên trong việc quyết định điều trị là loại đông cứng dáng đi này có gây khó chịu cho người bệnh hay không, tức là triệu chứng này có ảnh hưởng thế nào đến khả năng đi lại hay chất lượng cuộc sống của người bệnh. Tuy nhiên, triệu chứng đông cứng dáng đi dù nhẹ và không gây khó chịu cũng cần được xem xét quản lý đúng mức vì nó có thể nặng lên theo thời gian [27].
Điều trị đông cứng dáng đi nhẹ
Vật lý trị liệu và phục hồi chức năng bao gồm cả tập thể dục là phương pháp quan trọng giúp cải thiện vận động và phòng ngừa té ngã ở người bệnh đông cứng dáng đi. Do đó, nên có kỹ thuật viên vật lý trị liệu chuyên nghiệp hỗ trợ người bệnh. Các mẹo khi bước đi là những cách đơn giản cần được huấn luyện người bệnh khi có triệu chứng này. Một số mẹo điển hình[27]:
– Ngập ngừng lúc khởi đầu: chuyển trọng lượng cơ thể lên một chân trước khi bước chân kia lên.
– Ngập ngừng lúc xoay: xoay vòng lớn.
– Ngập ngừng khi qua chổ hẹp: tạo không gian rộng hơn.
– Ngập ngừng nơi đông người: tập kiểm soát lo lắng.
– Ngập ngừng khi làm công việc kép: tập trung vào bước chân.
– Di chuyển bằng xe đạp là một cách có hiệu quả để vượt qua đông cứng dáng đi.
Một số điều trị khác có thể được xem xét ở bệnh nhân đông cứng dáng đi nhẹ. Một trong số đó là sử dụng nhóm thuốc IMAOs như rasagiline và selegiline vì một số nghiên cứu nhỏ cho thấy dùng các thuốc này có thể giảm tiến triển nguy cơ đông cứng dáng đi[37, 38].
Điều trị đông cứng dáng đi nặng
Điều trị đông cứng dáng đi gây khó chịu phụ thuộc vào kiểu đông cứng dáng đi liên quan đến đáp ứng với dopaminergic.
Đông cứng dáng đi đáp ứng với dopaminergic (kiểu “tắt”)
Mục tiêu điều trị đầu tiên ở nhóm này là giảm ảnh hưởng của biến chứng dao động vận động lên đông cứng dáng đi bằng cách giảm thời gian “tắt” của người bệnh. Sử dụng nguyên tắc chung cho điều chỉnh biến chứng dao động vận động ở người bệnh Parkinson, trong đó điều chỉnh levodopa giữ vai trò chủ đạo như tăng liều levodopa, tăng số lần levodopa, hoặc dùng levodopa tác dụng kéo dài thế hệ mới. Trường hợp người bệnh chỉ đang dùng thuốc đồng vận dopamine, thuốc này có hiệu quả lên đông cứng dáng đi yếu hơn so với levodopa, đo đó có thể tăng liều đồng vận dopamine hoặc thêm levodopa[39]. Nếu dao động vận động đã cải thiện nhưng đông cứng dáng đi vẫn chưa giảm thì nên giảm liều đồng vận dopamine, đôi khi cần ngưng thuốc này vì chúng có thể lại là nguyên nhân gây đông cứng dáng đi. Nếu đông cứng dáng đi vẫn không cải thiện như mong muốn, có thể xem xét thêm amantadine vào điều trị, tuy nhiên bằng chứng cho điều trị này ở mức độ yếu[40].
Trong trường hợp đông cứng dáng đi giai đoạn “tắt” không đáp ứng với thuốc, điều trị xâm lấn có thể là một lựa chọn như truyền levodopa qua ruột liên tục[41] hoặc phẫu thuật kích thích não sâu nhân dưới đồi[42]. Kích thích não sâu nhân dưới đồi với tần số thấp 60Hz ghi nhận có hiệu quả hơn khi so với tần số cao[43]. Tuy nhiên, bằng chứng của các kỹ thuật xâm lấn này trong điều trị đông cứng dáng đi có mức độ yếu. Một số trường hợp đông cứng dáng đi không cải thiện sau phẫu thuật kích thích não sâu, việc sử dụng methylphenidate có thể giúp cải thiện triệu chứng này[33].
Đông cứng dáng đi kháng trị với dopaminergic (Kiểu “tắt – bật”) Levodopa là thuốc điều trị chính cho bệnh nhân đông cứng dáng đi thuộc nhóm này cho cả levodopa uống và truyền qua ruột[44]. Các thuốc khác chưa ghi nhận hiệu quả. Phẫu thuật kích thích não sâu vùng nhân cuống cầu (PPN) được ghi nhận có hiệu quả yếu và chỉ nên thực hiện ở những trung tâm có kinh nghiệm[45].
Đông cứng dáng đi gây ra do dopaminergic (kiểu “bật”) Đông cứng dáng đi gây ra do dopaminergic chủ yếu được điều trị bằng cách giảm các thuốc dopaminergic. Đồng vận dopamine nên được giảm trước tiên, tiếp theo là levodopa. Khi cần thiết phải giảm các thuốc dopaminergic mà làm ảnh hưởng đến việc kiểm soát các triệu chứng chính khác của bệnh Parkinson thì phẫu thuật kích thích não sâu là phương pháp điều trị thay thế. Việc điều trị này không tác động trực tiếp vào triệu chứng đông cứng dáng đi, mà nó ảnh hưởng gián tiếp thông qua việc thay thế hiệu quả và tác dụng phụ của thuốc[27].
Điều trị không dùng thuốc Vật lý trị liệu và phục hồi chức năng được ghi nhận có hiệu quả trong đông cứng dáng đi ở các giai đoạn[46]. Điều trị bao gồm các thành phần tương tự như điều trị đông cứng dáng đi nhẹ. Sử dụng các dụng cụ hỗ trợ mẹo cảm giác như dụng cụ chiếu đèn lazer (gậy, giày, xe đẩy…), dụng cụ tạo âm thanh để bước theo nhịp, dụng cụ kích thích cảm giác. Ngoài ra, đông cứng dáng đi bị ảnh hưởng bởi những hạn chế trong môi trường hoạt động, một nhà trị liệu nghề nghiệp là cần thiết để cho lời khuyên về khả năng thích ứng công việc, chẳng hạn như loại bỏ các chướng ngại vật, tối ưu hóa ánh sáng hoặc thiết kế các lối đi an toàn. Hơn nữa, đông cứng dáng đi có thể tăng lên trong các tình huống căng thẳng và các nhà trị liệu nghề nghiệp có thể hỗ trợ lập kế hoạch, lịch trình hàng ngày, nhằm giảm thiểu căng thẳng[22, 27].
Điều trị bệnh kèm theo Nhiều bệnh kèm theo có thể ảnh hưởng bất lợi đến dáng đi như bệnh về thị giác, bệnh cơ xương khớp… Do đó những bệnh lý này cần được quan tâm và điều trị đúng mức [27].
Kết luận
Đông cứng dáng đi trong bệnh Parkinson là một trông những triệu chứng vận động gây tàn phế nặng nhưng còn nhiều hạn chế trong chẩn đoán và điều trị. Cùng với sự tiến bộ về kỹ thuật y học và những hiểu biết về cơ chế sinh bệnh của đông cứng dáng đi, hy vọng sẽ có nhiều nghiên cứu chẩn đoán và điều trị có hiệu quả trong tương lai.
Tài liệu tham khảo
1. Kaliva LV, L.A., Parkinson’s Disease. Lancet Neurol, 2015. 386(9996): p. 896-912.
2. Sveinbjornsdottir, S., The clinical symptoms of Parkinson’s disease. J Neurochem, 2016. 139 Suppl 1: p. 318-324.
3. Mirelman, A., et al., Gait impairments in Parkinson’s disease. Lancet Neurol, 2019. 18(7): p. 697-708.
4. Morris, M.E., et al., The pathogenesis of gait hypokinesia in Parkinson’s disease. Brain, 1994. 117 ( Pt 5): p. 1169-81.
5. Bloem, B.R., et al., Falls and freezing of gait in Parkinson’s disease: a review of two interconnected, episodic phenomena. Mov Disord, 2004. 19(8): p. 871-84.
6. Schaafsma, J.D., et al., Characterization of freezing of gait subtypes and the response of each to levodopa in Parkinson’s disease. Eur J Neurol, 2003. 10(4): p. 391-8.
7. Walton, C.C., et al., The major impact of freezing of gait on quality of life in Parkinson’s disease. J Neurol, 2015. 262(1): p. 108-15.
8. Okuma, Y., et al., A prospective study of falls in relation to freezing of gait and response fluctuations in Parkinson’s disease. Parkinsonism Relat Disord, 2018. 46: p. 30-35.
9. Gilat, M., et al., Freezing of gait: Promising avenues for future treatment. Parkinsonism Relat Disord, 2018. 52: p. 7-16.
10. Bohnen, N.I., et al., Extra-nigral pathological conditions are common in Parkinson’s disease with freezing of gait: an in vivo positron emission tomography study. Mov Disord, 2014. 29(9): p. 1118-24.
11. Moore, O., C. Peretz, and N. Giladi, Freezing of gait affects quality of life of peoples with Parkinson’s disease beyond its relationships with mobility and gait. Mov Disord, 2007. 22(15): p. 2192-5.
12. Sun, Q., et al., Clinical Profile of Chinese Long-Term Parkinson’s Disease Survivors With 10 Years of Disease Duration and Beyond. Aging Dis, 2018. 9(1): p. 8-16.
13. Ge, H.-L., et al., The prevalence of freezing of gait in Parkinson’s disease and in patients with different disease durations and severities. Chinese Neurosurgical Journal, 2020. 6(1): p. 17.
14. Gan, J., et al., Prevalence and Clinical Features of FOG in Chinese PD Patients, a Multicenter and Cross-Sectional Clinical Study. Frontiers in Neurology, 2021. 12(216).
15. Ružickaˇ E, J.J., Disorders of gait, in Parkinson’s disease and movement disorders, T.E. Jankovic JJ, editors, Editor. 2002, Lippincott,Williamsand Wilkins: Philadelphia. p. 409-29.
16. Marquez, J.S., et al., Neural Correlates of Freezing of Gait in Parkinson’s Disease: An Electrophysiology Mini-Review. Frontiers in Neurology, 2020. 11(1303).
17. M Amboni, F.S., G Abbruzzese et al., Prevalence and associated features of self-reported freezing of gait in Parkinson disease: The DEEP FOG study. Parkinsonism & Related Disorders, 2015. 21(6): p. 644-9.
18. Santiago Perez-Lloret, L.N.-P., Philippe Damier et al., Prevalence, determinants, and effect on quality of life of freezing of gait in Parkinson disease. JAMA Neurol, 2014. 71(7): p. 884-90.
19. Ortelli, P., et al., How Cognition and Motivation “Freeze” the Motor Behavior in Parkinson’s Disease. Frontiers in neuroscience, 2019. 13: p. 1302.
20. Choi, S.-M., et al., Factors associated with freezing of gait in patients with Parkinson’s disease. Neurological Sciences, 2019. 40(2): p. 293-298.
21. Forsaa, E., et al., A 12-year population-based study of freezing of gait in Parkinson’s disease. Parkinsonism & related disorders, 2015. 21(3): p. 254-258.
22. Chao Gao, J.L., Yuyan Tan and Shengdi Chen, REVIEW: Freezing of gait in Parkinson’s disease: pathophysiology, risk factors and treatments. Translational NeuroDegeneration, 2020(9): p. 12.
23. Giladi, N., F.B. Horak, and J.M. Hausdorff, Classification of gait disturbances: distinguishing between continuous and episodic changes. Mov Disord, 2013. 28(11): p. 1469-73.
24. Schaafsmaa, JD., et al. Characterization of freezing of gait subtypes and the response of each to levodopa in Parkinson’s disease. European Journal of Neurology, 2003. 10.
25. Dean Sweeney, L.R.Q., Patrick Browne, A Technological Review of Wearable Cueing Devices Addressing Freezing of Gait in Parkinson’s Disease. Journal of Sensors, 2019.
26. Claudia Barthel, E.M., Bettina Debu, The Practicalities of Assessing Freezing of Gait. Journal of Parkinson’s Disease, 2016. 6: p. 667-674.
27. Nonnekes, J., et al., Freezing of gait: a practical approach to management. The Lancet Neurology, 2015. 14(7): p. 768-778.
28. Goetz, C.G., et al., Movement Disorder Society-sponsored revision of the Unified Parkinson’s Disease Rating Scale (MDS-UPDRS): scale presentation and clinimetric testing results. Mov Disord, 2008. 23(15): p. 2129-70.
29. Giladi, N., et al., Validation of the freezing of gait questionnaire in patients with Parkinson’s disease. Mov Disord, 2009. 24(5): p. 655-61.
30. Nieuwboer, A., et al., Reliability of the new freezing of gait questionnaire: agreement between patients with Parkinson’s disease and their carers. Gait Posture, 2009. 30(4): p. 459-63.
31. Ziegler, K., et al., A new rating instrument to assess festination and freezing gait in Parkinsonian patients. Mov Disord, 2010. 25(8): p. 1012-8.
32. Snijders, A.H., et al., Freezer or non-freezer: clinical assessment of freezing of gait. Parkinsonism Relat Disord, 2012. 18(2): p. 149-54.
33. Moreau, C., et al., Methylphenidate for gait hypokinesia and freezing in patients with Parkinson’s disease undergoing subthalamic stimulation: a multicentre, parallel, randomised, placebo-controlled trial. Lancet Neurol, 2012. 11(7): p. 589-96.
34. Giladi, N. and T. Herman, How Do I Examine Parkinsonian Gait? Movement Disorders Clinical Practice, 2016. 3(4): p. 427-427.
35. Delval, A., et al., Characterization and quantification of freezing of gait in Parkinson’s disease: Can detection algorithms replace clinical expert opinion? Neurophysiol Clin, 2015. 45(4-5): p. 305-13.
36. Sweeney, D., et al., A Technological Review of Wearable Cueing Devices Addressing Freezing of Gait in Parkinson’s Disease. Sensors (Basel), 2019. 19(6).
37. Rascol, O., et al., Rasagiline as an adjunct to levodopa in patients with Parkinson’s disease and motor fluctuations (LARGO, Lasting effect in Adjunct therapy with Rasagiline Given Once daily, study): a randomised, double-blind, parallel-group trial. Lancet, 2005. 365(9463): p. 947-54.
38. Giladi, N., et al., Freezing of gait in PD: prospective assessment in the DATATOP cohort. Neurology, 2001. 56(12): p. 1712-1721.
39. Rascol, O., et al., A five-year study of the incidence of dyskinesia in patients with early Parkinson’s disease who were treated with ropinirole or levodopa. N Engl J Med, 2000. 342(20): p. 1484-91.
40. Lee, J.Y., et al., Intravenous amantadine on freezing of gait in Parkinson’s disease: a randomized controlled trial. J Neurol, 2013. 260(12): p. 3030-8.
41. Rispoli, V., et al., Levodopa/Carbidopa Intestinal Gel Infusion Therapy: Focus on Gait and Balance. Mov Disord Clin Pract, 2018. 5(5): p. 542-545.
42. Vercruysse, S., et al., Effects of deep brain stimulation of the subthalamic nucleus on freezing of gait in Parkinson’s disease: a prospective controlled study. J Neurol Neurosurg Psychiatry, 2014. 85(8): p. 871-7.
43. Xie, T., et al., Effect of low versus high frequency stimulation on freezing of gait and other axial symptoms in Parkinson patients with bilateral STN DBS: a mini-review. Transl Neurodegener, 2017. 6: p. 13.
44. Chang, F.C., et al., 24 h Levodopa-carbidopa intestinal gel may reduce falls and “unresponsive” freezing of gait in Parkinson’s disease. Parkinsonism Relat Disord, 2015. 21(3): p. 317-20.
45. Thevathasan, W., et al., Pedunculopontine nucleus deep brain stimulation in Parkinson’s disease: A clinical review. Mov Disord, 2018. 33(1): p. 10-20.
46. Cosentino, C., et al., Effectiveness of Physiotherapy on Freezing of Gait in Parkinson’s Disease: A Systematic Review and Meta-Analyses. Mov Disord, 2020. 35(4): p. 523-536.