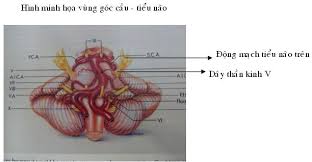
Các rối loạn Thần kinh thực vật trong bệnh teo da hệ thống thể tiểu não
Võ Nguyễn Ngọc Trang, Cù Mỹ Hiếu Hạnh, Nguyễn Thanh Huy
Trần Quang Tuyến, Nguyễn Hữu Công
Bệnh viện Ngoại Thần kinh Quốc tế
TÓM TẮT
Mở đầu: Teo đa hệ thống thể tiểu não (MSA-C) ảnh hưởng đến hệ tiểu não và thần kinh thực vật. Rối loạn thực vật đóng vai trò quan trọng trong chẩn đoán bệnh. Khảo sát test thần kinh thực vật giúp khách quan hóa các triệu chứng rối loạn thực vật trên lâm sàng.
Mục tiêu: Khảo sát đặc điểm các test thần kinh thực vật trong bệnh MSA-C.
Phương pháp: Báo cáo hàng loạt ca.
Kết quả: Trong 10 trường hợp MSA-C (7 nam, 3 nữ, tuổi trung bình 56,3 ± 2,8), có 6/10 thỏa tiêu chuẩn chẩn đoán “rất có thể MSA” và 4/10 trường hợp “có thể MSA”, dựa trên tiêu chuẩn chẩn đoán đồng thuận về bệnh teo đa hệ thống của Hoa Kỳ. Tỷ lệ bất thường của các test thần kinh thực vật bao gồm test thay đổi huyết áp theo tư thế, chỉ số 30:15, test thay đổi nhịp tim khi hít thở sâu, test vận động thể lực đẳng trường, test thay đổi huyết áp khi kích thích lạnh, và test ghi đáp ứng giao cảm da lần lượt là 70%, 30%, 75%, 70 %, 50% và 70%. Bất thường cao nhất là ở test thay đổi nhịp tim khi hít thở sâu.
Kết luận: Trong bệnh lý teo đa hệ thống thể tiểu não, thấy có bất thường các test thần kinh thực vật, với tỷ lệ thay đổi từ 30 – 75%, và cao nhất là ở test thay đổi nhịp tim khi hít thở sâu.
Từ khóa: test thần kinh thực vật, bệnh lý teo đa hệ thống, hội chứng tiểu não.
I. ĐẶT VẤN ĐỀ
Bệnh teo đa hệ thống (multiple system atrophy – MSA) là một bệnh thoái hóa thần kinh, tăng tiến dần với các triệu chứng của parkinson, thất điều tiểu não, suy giảm chức năng thực vật, rối loạn chức năng niệu – sinh dục, và bệnh lý của bó vỏ gai. Bệnh thường khởi phát ở người lớn tuổi, với triệu chứng lâm sàng ban đầu là rối loạn cơ vòng (tiểu dầm, rối loạn cương). Bệnh được phân chia thành 2 phân nhóm chính là nhóm với triệu chứng tiểu não ưu thế (cerebellar type MSA, MSA-C) và nhóm với triệu chứng parkinson ưu thế (parkinsonian type MSA MSA-P). Trước đây, bệnh MSA và liệt trên nhân tiến triển (Progressive Supranuclear Palsy – PSP), cùng với bệnh thoái hóa hạch nền – vỏ não (Corticobasal Degeneration – CBD) hay được gọi chung là nhóm các hội chứng Parkinson cộng thêm (Parkinson – Plus syndromes), vì có nhiều triệu chứng gần giống Parkinson nhưng có kèm thêm những triệu chứng khác với bệnh Parkinson nguyên phát. Giải phẫu bệnh của MSA – C gồm có thoái hóa ưu thế ở trám – cầu – tiểu não, dư thừa số lớn các thể vùi trong bào tương của các tế bào thần kinh đệm. Các thể vùi (inclusion) là do các protein a-synuclein xoắn lại thành sợi tạo ra. Về mặt giải phẫu bệnh, bệnh MSA cùng với bệnh Parkinson và bệnh sa sút trí tuệ do thể Lewy được coi như có chung bản chất là rối loạn của a-synuclein, và được gọi là bệnh của a-synuclein (a-synucleinnopathy).
Năm 2008, các chuyên gia về MSA, bao gồm các nhà lâm sàng, bệnh lý học, và hình ảnh học, đã thống nhất bản đồng thuận về các tiêu chuẩn chẩn đoán MSA-C của Hội Thần Kinh Hoa Kỳ và Hội Thần Kinh Thực Vật Hoa Kỳ [10], bao gồm các bảng như trình bày sau đây.
Bảng 1: Tiêu chuẩn chẩn đoán “rất có thể là MSA” (probable MSA)
| Bệnh khởi phát ở người lớn trên 30 tuổi, tăng tiến dần, phân bố bệnh rải rác, với đặc điểm sau: |
|
Bảng 2 Tiêu chuẩn chẩn đoán “có thể MSA” (possible MSA):
| bệnh khởi phát ở người lớn trên 30 tuổi, tăng tiến dần, phân bố bệnh rải rác, với đặc điểm sau: |
|
Bảng 3: Các dấu hiệu bổ xung của “có thể là MSA”:
| Có thể MSA-P hoặc MSA-C |
|
| Có thể MSA-C |
|
Như vậy chẩn đoán chắc chắn bệnh MSA-C chỉ thực hiện được qua giải phẫu bệnh. Nếu chỉ dựa trên lâm sàng và hình ảnh học, chỉ có thể chẩn đoán MSA-C ở mức độ “rất có thể” và “có thể”.
Theo bản đồng thuận 2008, các test điện sinh lý giúp khảo sát được mức độ bị rối loạn chức năng của tuyến mồ hôi, và hệ tim mạch [10]. Một trong những dấu hiệu lâm sàng gợi ý MSA trên một bệnh nhân có triệu chứng giống parkinson là sớm té ngã. Té ngã trong MSA-C có thể chủ yếu do hội chứng tiểu não, tuy nhiên bất thường thần kinh thực vật cũng có thể đóng vai trò quan trọng. Khảo sát test thần kinh thực vật là một phương pháp không xâm lấn, có đủ độ nhạy trong việc phát hiện các bất thường trước khi triệu chứng lâm sàng xuất hiện [15].
Cho tới nay tại Việt Nam, theo hiểu biết của chúng tôi, vẫn chưa có nghiên cứu nào đi sâu vào nhóm bệnh MSA nói chung, cũng như MSA-C nói riêng, cũng chưa thấy có công trình nào đề cập đến các test thần kinh thực vật một cách đầy đủ hệ thống.
Mục tiêu của nghiên cứu này là bước đầu khảo sát các test thần kinh thực vật trong bệnh MSA-C.
PHƯƠNG PHÁP NGHIÊN CỨU
Thiết kế và đối tượng nghiên cứu: Nghiên cứu mô tả loạt ca (case series), khảo sát các triệu chứng lâm sàng và cận lâm sàng của các bệnh nhân tạibệnh viện Ngoại Thần Kinh Quốc Tế, từ 8/2012 đến 8/2013, và lựa chọn bệnh nhân thỏa tiêu chuẩn đồng thuận năm 2008. Nhịp tim tại từng thời điểm được tính toán thông qua khoảng cách giữa 2 đỉnh sóng R của điện tim.
Các test khảo sát chức năng thần kinh thực vật:
2.1. Test biến thiên nhịp tim & huyết áp khi thay đổi tư thế: Đo huyết áp và nhịp tim ở tư thế nằm, sau đó bắt đầu cho bệnh nhân đứng dậy. Đo huyết áp ở phút thứ 2 và thứ 5 sau khi đứng dậy.Tìm biến thiên huyết áp khi nằm so với khi đứng. Tỷ số 30:15 = khoảng R-R của nhịp tim thứ 30 sau khi đứng/ khoảng R-R của nhịp tim thứ 15 sau khi đứng [2] [9]
2.2. Test biến thiên nhịp tim khi hít thở sâu: Cho bệnh nhân hít thở sâu 6 lần trong vòng 1 phút, tìm biến thiên nhịp tim giữa hít vào và thở ra [2] [9]
2.3. Test biến thiên huyết áp khi vận động thể lực đẳng trường: Cho bệnh nhân nắm giữ máy đo huyết áp trong 3 phút sao cho duy trì áp lực bằng 1/3 áp lực bóp tay tối đa của chính bệnh nhân. Tìm biến thiên huyết áp khi gắng sức đẳng trường so với khi nghỉ ngơi [9]
2.4. Test biến thiên huyết áp với thụ thể lạnh: Đặt 2 túi nước đá trên và dưới bàn tay bệnh nhân trong 90 giây. Tìm biến thiên huyết áp khi kích thích lạnh so với khi nghỉ ngơi [8]
2.5. Test ghi đáp ứng giao cảm da: Đặt điện cực ghi trên da ở bàn chân và bàn tay, khi có biến đổi của tuyến mồ hôi do kích thích gây nên, thì điện trở da sẽ thay đổi. Kích thích được thực hiện bằng đá lạnh và kích thích điện vào dây thần kinh.
2.6. Chúng tôi không thực hiện nghiệm pháp Valsalva. Vì lý do kỹ thuật, chúng tôi cũng không thực hiện các test mồ hôi điều nhiệt (thermoregulatory sweat test), phản xạ sợi trục tiết mồ hôi định tính (Quantitative sudomotor axon reflex test – QSART) và cảm giác định lượng (Quantitative sensory test – QST).
Phương tiện: máy điện cơ VikingQuest (Nicolet) Vyasis 4 kênh.
Phương pháp xử lý số liệu: thống kê mô tả
KẾT QUẢ NGHIÊN CỨU
Trong thời gian 1 năm (từ 8-2012 tới 8-2013), chúng tôi khảo sát được 10 trường hợp teo đa hệ thống thể tiểu não (MSA-C), gồm 6 nam và 4 nữ. Trong đó có 6 trường hợp thỏa tiêu chuẩn chẩn đoán “rất có thể là MSA” và 4 trường hợp thỏa tiêu chuẩn “có thể là MSA”. Tuổi trung bình tại thời điểm chẩn đoán là 56,3 tuổi (SD = 2,8).
3.1. Các thông số của các test thần kinh thực vật trên các bệnh nhân MSA-C:
Bảng 1: Các test khảo sát chức năng phó giao cảm
| Test khảo sát | Trung bình |
| Biến thiên nhịp tim với hít thở sâu (Respiratory sinus arrythmia) | 9,1 |
| Biến thiên nhịp tim với tư thế – Chỉ số 30:15 (30:15 ratio) | 1,1 |
(Có 2 trường hợp không thực hiện được nghiệm pháp hít thở sâu)
Nhận xét: Chỉ số 30:15 trung bình = 1,1 > 1, có tăng nhịp tim khi đứng so với khi nằm. Khi hít vào và thở ra, thay đổi nhịp tim trung bình là 9,1 nhịp/phút.
Bảng 2: Các test khảo sát chức năng giao cảm tim mạch
| Test khảo sát | Biến thiên huyết áp (mmHg) | ||
| Tâm thu | Tâm trương | ||
| Thụ thể lạnh (Cold pressure) | 10 | 3,7 | |
| Vận động thể lực đẳng trường(Isometric exercise – IET) | 10,4 | -2,8 | |
| Thay đổi tư thế(Standing blood pressure) | Phút 2 | -18 | -5,8 |
| Phút 5 | -14,6 | -9,6 | |
Nhận xét: Sau khi kích thích lạnh và vận động thể lực đẳng trường, có tăng huyết áp tâm thu. Khi thay đổi tư thế từ nằm sang đứng, thay đổi chủ yếu ở huyết áp tâm thu. Có giảm huyết áp tâm thu ở thời điểm 2 phút sau khi đứng, và sau 5 phút huyết áp vẫn còn giảm.
Bảng 3: Test ghi đáp ứng giao cảm da (Sympathetic skin response – SSR)
| Có | Không | |
| Đáp ứng với kích thích lạnh và điện | 3 | 7 |
Nhận xét: có 7 trong 10 trường hợp không đáp ứng hoặc đáp ứng rất kém với kích thích lạnh và kích thích điện vào dây thần kinh
3.2. Tỷ lệ bất thường các test thần kinh thực vật:
Bảng 4: Đặc điểm bất thường các test thần kinh thực vật
| Giao cảm | Phó giao cảm | Giao cảm & phó giao cảm | |
| Số trường hợp (N=10) | 2 | 0 | 8 |
| Tỷ lệ (%) | 20 | 0 | 80 |
Nhận xét: Trong 10 trường hợp khảo sát, có 2 trường hợp chỉ bất thường hệ giao cảm, còn lại 8 trường hợp bất thường ảnh hưởng trên cả hệ giao cảm và phó giao cảm, chiếm 80%.
Bảng 5: Tỷ lệ bất thường của các test thần kinh thực vật.
| Bất thường | Tỷ lệ (%) | |
| Chỉ số 30:15 (30 : 15 ratio) | 3/10 | 30 |
| Thay đổi tư thế (Standing blood pressure) | 7/10 | 70 |
| Hít thở sâu(Deep breathing) | 6/8 | 75 |
| Vận động thể lực đẳng trường (IET) | 7/10 | 70 |
| Kích thích lạnh (Cold pressor) | 5/10 | 50 |
| Ghi đáp ứng giao cảm da (SSR) | 7/10 | 70 |
Nhận xét: Tỷ lệ rối loạn thần kinh thực vật thay đổi tùy theo các test. Tỷ lệ bất thường cao nhất là ở biến thiên nhịp tim với hít thở sâu.
Bảng 6: Phân loại mức độ nặng rối loạn thần kinh thực vật
| Số test bất thường | Số trường hợp | Tỷ lệ (%) |
| 1 test | 1 | 10 |
| 2 test | 2 | 20 |
| 3 test | 0 | 0 |
| 4 test | 4 | 40 |
| 5 test | 3 | 30 |
| 6 test | 0 | 0 |
Nhận xét: Tất cả các trường hợp đều bất thường ở ít nhất 1 test khảo sát, trong đó chiếm tỷ lệ cao nhất là bất thường 4 test, chiếm 40%
BÀN LUẬN:
Mặc dù là một bệnh ít gặp, nhưng trong 1 năm chúng tôi đã có được 10 trường hợp bệnh teo đa hệ thống thể tiểu não, trong đó có 6 trường hợp thỏa tiêu chuẩn chẩn đoán “rất có thể là MSA” và 4 trường hợp “có thể là MSA”, điều đó chứng tỏ: dù là một bệnh ít gặp, nhưng ở tuyến chuyên khoa thì MSA-C không phải là quá hiếm, và nếu không lưu ý các triệu chứng thần kinh thực vật, sẽ rất dễ chẩn đoán nhầm một hội chứng tiểu não đơn thuần.
Khi tiến hành nghiên cứu này, chúng tôi không tìm được các nghiên cứu về các test thần kinh thực vật trên bệnh nhân Parkinson và MSA ở Việt Nam, do vậy chúng tôi không thể so sánh các kết quả của chúng tôi với các nghiên cứu trong nước. Rất có thể đây là nghiên cứu theo hướng này đầu tiên ở Việt Nam. Hoàng Trung Vinh và Lê Văn Bổn cũng có nghiên cứu một vài test thần kinh thực vật, nhưng chỉ ở bệnh nhân đái tháo đường típ 2.
Theo y văn thế giới, đã có nhiều báo cáo về các yếu tố dự đoán tiến triển và tiên lượng sống còn của bệnh teo đa hệ thống. Người ta thấy rối loạn thần kinh thực vật là yếu tố tiên lượng xấu ở bệnh nhân bị bệnh teo đa hệ thống [20] [21]. Rối loạn thần kinh thực vật trong bệnh teo đa hệ thống thường biểu hiện rõ rệt và nặng hơn so với trong bệnh Parkinson [13] [19].
Như trên đã nêu, các tác giả Hoàng Trung Vinh và Lê Văn Bổn đã nghiên cứu biến chứng thần kinh thực vật ở bệnh nhân đái tháo đường típ 2. Tuy nhiên các tác giả chỉ khảo sát các test đánh giá chức năng thần kinh thực vật tim mạch, gồm biến thiên nhịp tim với các kích thích khác nhau và biến thiên huyết áp từ nằm sang đứng [1] [3]. Phòng điện cơ của bệnh viện chúng tôi có thể thực hiện được gần đầy đủ các test khảo sát chức năng thần kinh thực vật, tương tự như ở các phòng điện cơ tại một số nước tiên tiến [4] [6] [9] [12] [18]. Ngoài các test về thần kinh thực vật của tim mạch, chúng tôi còn khảo sát thêm các test đánh giá chức năng hệ giao cảm, bao gồm: test ghi đáp ứng giao cảm da, test thay đổi huyết áp khi vận động thể lực đẳng trường và với kích thích lạnh. Tuy nhiên, chúng tôi không có phương tiện để làm một số test chuyên sâu như trong mục 2.6 đã nêu. Chúng tôi tạm thời chưa thực hiện nghiệm pháp Valsalva, vì có nguy cơ ngất hoặc rối loạn nhịp, đặc biệt là trên nhóm đối tượng đã có bệnh lý về tim mạch [17] [16]
4.1. Các thông số của các test thần kinh thực vật trên các bệnh nhân MSA
Bảng 8: So sánh các thông số của các test thần kinh thực vật giữa các nghiên cứu
| Biến thiên nhịp tim (nhịp/phút) | Biến thiên huyết áp (mmHg) | ||||
| Chỉ số30:15 | Hít thở sâu | Thay đổi tư thế | Vận động thể lực | Kích thích lạnh | |
| Chúng tôi, (n=10) | 1,1 | 9,1 | -18 | 10,4 | 10 |
| Riley, (n = 13) | 4,18 | -47 | |||
| Kimber, (n = 20) | 3 | -66 | 9 | 12 | |
| Bonuccelli, (n = 5) | 1,3 | 16 | -24,8 | 24,8 | |
Chú thích: tác giả nước ngoài thực hiện test cả MSA-C lẫn MSA-P, số liệu của chúng tôi chỉ tính cho MSA-C.
Chúng tôi thấy có rối loạn chức năng giao cảm ở bệnh nhân bị MSA-C, biểu hiện bằng hiện tượng giảm huyết áp tâm thu ở thời điểm 2 phút sau khi đứng và sau 5 phút, huyết áp vẫn tiếp tục giảm nhiều hơn so với 2 phút. Trong 10 bệnh nhân, có 7 trường hợp bất thường, trong đó 5 trường hợp thỏa tiêu chuẩn chẩn đoán “rất có thể là MSA” với huyết áp tâm thu giảm trên 30mmHg hoặc huyết áp tâm trương giảm trên 15mmHg. Tác giả Riley khảo sát test bàn nghiêng cho 13 trường hợp teo đa hệ thống tại Hoa Kỳ, độ giảm huyết áp tâm thu trung bình là 47mmHg, tác giả Kimber khảo sát 20 trường hợp teo đa hệ thống tại Anh, cũng ghi nhận độ giảm huyết áp tâm thu rất rõ, trung bình là 66mmHg [12] [18]. Kết quả của hai nghiên cứu này cho thấy bệnh nhân teo đa hệ thống tụt huyết áp tư thế rõ hơn so với trong nghiên cứu của chúng tôi. Nguyên nhân có thể vì chúng tôi không có điều kiện sử dụng bàn nghiêng. Bonuccelli ở Ý cũng không sử dụng bàn nghiêng, mà cho bệnh nhân tự đứng dậy, thì độ giảm huyết áp tâm thu cũng ít hơn, chỉ 24,8mmHg, gần tương tự như chúng tôi [6]. Chúng tôi có 3 trường hợp bất thường về chỉ số 30:15, phản ánh rối loạn chức năng phó giao cảm liên quan thay đổi nhịp tim khi đứng so với khi nằm.
Bình thường, khi hít vào sâu thì nhịp tim tăng lên, khi thở ra nhịp tim giảm [2]. Chúng tôi lấy trung bình 6 khoảng R-R dài nhất trong 6 lần thở ra và trung bình của 6 khoảng R-R ngắn nhất trong 6 lần hít vào liên tục, từ đó tính ra chênh lệch nhịp tim giữa hít vào và thở ra. Biến thiên ở người bình thường khỏe mạnh là 15 nhịp/phút [8] [9]. Nếu biến thiên dưới mức đó, được coi là có rối loạn phó giao cảm. Trong 10 bệnh nhân, có 2 trường hợp không thực hiện được nghiệm pháp hít thở sâu, 8 trường hợp có biến thiên nhịp tim trung bình là 9,1 nhịp/phút. Mức độ biến thiên này thấp hơn so với nghiên cứu của tác giả Bonuccelli, và cao hơn so với nghiên cứu của Riley (4,18 nhịp/phút) và Kimber (3 nhịp/phút) [12] [18]. Nguyên nhân có thể do chúng tôi chỉ tính riêng trên MSA-C, và không tính cho những người được chẩn đoán MSA-P, cũng có thể do các cỡ mẫu còn nhỏ, và do cách thực hiện hơi khác nhau.
Sau khi vận động thể lực đẳng trường, có 7 trường hợp test bất thường, trong đó 6 trường hợp huyết áp giảm hoặc thay đổi không đáng kể và 1 trường hợp còn lại thì huyết áp tăng 60mmHg, vượt ngưỡng bình thường. Có 5 trường hợp không có thay đổi huyết áp đáng kể sau kích thích lạnh. Kết quả này phù hợp với một nghiên cứu tại Anh, chứng tỏ có sự bất thường chức năng giao cảm trên bệnh nhân MSA [12].
Trong nhóm bệnh nhân MSA-C của chúng tôi, test ghi đáp ứng giao cảm da bất thường ở trên 7 bệnh nhân, biểu hiện bằng không đáp ứng hoặc đáp ứng rất kém với kích thích lạnh và điện, cũng chứng tỏ có bất thường chức năng giao cảm.
4.2. Tỷ lệ bất thường các test thần kinh thực vật:
Như bảng 4 (mục 3.2) đã nêu, khi khảo sát các test thần kinh thực vật trên 10 bệnh nhân MSA, thấy có rối loạn chức năng cả của hệ giao cảm lẫn hệ phó giao cảm. Kết quả này phù hợp với nhiều nghiên cứu đã được báo cáo [6] [18]. Có 6 test thần kinh thực vật được thực hiện, và kết quả cho thấy tỷ lệ bất thường thay đổi trong khoảng 30 – 75% tùy theo các test.
Bảng 7 : So sánh tỷ lệ bất thường các test thần kinh thực vật giữa các nghiên cứu
| Phó giao cảm | Giao cảm | |||||
| Chỉ số30:15 | Hít thở sâu | Thay đổitư thế | Vận động thể lực | Kích thích lạnh | Đáp ứnggiao cảm da | |
| Chúng tôi, (n = 12) | 30% | 75% | 70% | 70% | 50% | 70% |
| Riley DE, (n =13) | 84,6% | 76,9% | ||||
| Bordet R, (n =13) | 69% | |||||
| Asahina, (n = 40) | 32,5% | 45% | 47,5% | |||
| Albanese, (n = 15) | 70% | 70% | 30% | 30% | ||
| Tada M, (n = 49) | 76% | |||||
Chú thích: tác giả nước ngoài thực hiện test cả MSA-C lẫn MSA-P, số liệu của chúng tôi chỉ tính cho MSA-C.
Tỷ lệ bất thường test ghi đáp ứng giao cảm da trong nghiên cứu tương đương với của Bordet và cao hơn so với Asahina [5] [7] . Bất thường cao nhất là ở test thay đổi nhịp tim với nghiệm pháp hít thở sâu, với tỷ lệ 75%, phù hợp với tác giả Albanese, nhưng thấp hơn so với của Riley [18] [4]. Về test thay đổi huyết áp khi thay đổi tư thế, tỷ lệ bất thường cao hơn so với của Asahina và Albanese [5] [4]. Tuy nhiên, tỷ lệ này lại thấp hơn so với của Riley và Tada [18] [20]. Test thay đổi huyết áp khi thay đổi tư thế với huyết áp tâm thu giảm trên 30mmHg hoặc huyết áp tâm trương giảm trên 15mmHg là 1 trong 3 đặc điểm chẩn đoán “rất có thể teo đa hệ thống” trong tiêu chuẩn đồng thuận của Hội Thần Kinh Hoa Kỳ và Hội Thần Kinh Thực Vật Hoa Kỳ [10]. Y văn cũng ghi nhận test này có độ nhạy cao trong việc phát hiện bất thường về thần kinh thực vật với tỷ lệ bất thường trên 75% [18] [20]. Trong nghiên cứu của chúng tôi tỷ lệ này chỉ là 70 %. Tỷ lệ bất thường về biến thiên nhịp tim khi thay đổi tư thế (chỉ số 30:15) trong nghiên cứu của chúng tôi cũng thấp hơn nghiên cứu trên Thế giới [4]. Nguyên nhân của sự khác biệt này, như phần trên đã nêu, có thể do chúng tôi không sử dụng nghiệm pháp bàn nghiêng khi thực hiện test.
Có nhiều bảng phân loại mức độ nặng dựa trên các test. Trong đó, sử dụng phổ biến là bảng phân loại của Ewing năm 1985 với 5 test, bao gồm 3 test khảo sát biến thiên nhịp tim (theo tư thế, hít thở sâu, Valsalva) và 2 test khảo sát biến thiên huyết áp (theo tư thế, vận động thể lực). Dựa vào số test bất thường và mức độ bất thường, tác giả phân thành các nhóm: bình thường, bất thường sớm, bất thường rõ rệt và bất thường nặng nề. Chúng tôi thực hiện 6 test và đánh giá mức độ nặng dựa vào số test bất thường trong 6 test khảo sát. Kết quả cho thấy tất cả các trường hợp khảo sát đều bất thường ở ít nhất 1 test khảo sát, trong đó chiếm tỷ lệ cao nhất là bất thường 4 test, chiếm 70%; có 3 trường hợp bất thường 5 test, chiếm 30%. Tác giả Albanese khảo sát các test thần kinh thực vật trong 15 trường hợp MSA, kết quả có 8 trường hợp bất thường nặng và 2 trường hợp bất thường rõ [4]. Như vậy, nghiên cứu của chúng tôi có phần phù hợp với tác giả cũng như y văn, rối loạn thần kinh thực vật trong bệnh teo đa hệ thống thể tiểu não thường biểu hiện rõ rệt và nặng [13] [19]. Tuy nhiên, cỡ mẫu của chúng tôi còn hạn chế, cần có nghiên cứu với cỡ mẫu lớn hơn và so sánh với bệnh Parkinson và các hội chứng Parkinson khác.
Có thể thấy các test thần kinh thực vật bất thường đã khách quan hóa và giải thích cho các triệu chứng lâm sàng như rối loạn cương, rối loạn cơ vòng bàng quang (tiểu dầm). Triệu chứng té ngã trong bệnh teo đa hệ thống thể tiểu não, không những có thể do bệnh lý tiểu não, mà còn có thể do rối loạn thần kinh thực vật.
5. KẾT LUẬN
5.1. Qua nghiên cứu trên 10 bệnh nhân bị bệnh teo đa hệ thống thể tiểu não (MSA-C), chúng tôi thấy có bất thường của các test thần kinh thực vật, biểu hiện trên cả hệ giao cảm và phó giảm.
5.2. Tỷ lệ rối loạn thần kinh thực vật trong nghiên cứu thay đổi từ 30 – 75 %, bất thường cao nhất là ở test thay đổi nhịp tim khi hít thở sâu.
5.3. Đây có thể là nghiên cứu đầu tiên ở Việt Nam về các test thần kinh thực vật trên một nhóm các bệnh nhân bị Parkinson cộng thêm. Trong tương lai cần có những nghiên cứu với mẫu lớn hơn.
AUTONOMIC FUNCTION TESTS IN
CEREBELLAR TYPE MULTIPLE SYSTEM ATROPHY DISEASE
ABSTRACT
Background: Multiple System Atrophy – cerebellar (MSA-C) involves the cerebellum and autonomic nervous systems. Autonomic failure is a part of the criteria for the diagnosis. Autonomic function tests help to objectify clinical dysautonomic signs.
Objectives: To characterise the profile autonomic dysfunctions in MSA-C
Methods: A case series study.
Results: Among 10 patients (7 men, 3 women, mean age 56.3 ± 2.8 years)with cerebellar type MSA (MSA-C), diagnosis was probable MSA in 6 cases and possible MSA in 4 the rest, based on the Second Consensus Statement on the Diagnosis of Multiple Systemic Atrophy. The rates of abnormalityfound in standing blood pressure test, 30:15 ratio, heart rate variability to deep breathing, isometric exercise, cold pressor, and sympathetic skin response were70%, 30%, 75%, 70 %, 50% và 70%, consecutively. The highest rate of abnormality was with RR interval variability to deep breathing test.
Conclusions: Abnormal values of autonomic function tests were revealed in MSA-C patients, ranging from 30% to 75% with the highest rate in the heart rate variability to deep breathing test.
Key words: autonomic function test, multiple system atrophy, cerebellar.
TÀI LIỆU THAM KHẢO
TIẾNG VIỆT
1. Lê Văn Bổn (2007), “Biến chứng thần kinh tự chủ tim mạch ở bệnh nhân đái tháo đường típ 2”, Luận án chuyên khoa 2, Đại học Y Dược TPHCM.
2. Nguyễn Hữu Công (2013), “Chẩn đoán điện và ứng dụng lâm sàng”, Nhà xuất bản Đại Học Quốc gia TP. Hồ Chí Minh, tr. 91 – 95
3. Hoàng Trung Vinh (2005), “Nghiên cứu thần kinh tự chủ tim mạch và mối liên quan với thời gian phát hiện bệnh, chỉ số khối cơ thể ở bệnh nhân đái tháo đường týp 2”. Tạp chí Nghiên cứu Y học, 4, tr. 38 – 41.
TIẾNG ANH
4. Albanese A, Colosimo C, Bentivoglio A R, Fenici R, Melillo G, et al. (1995), “Multiple system atrophy presenting as parkinsonism: clinical features and diagnostic criteria”. Journal of Neurology, Neurosurgery & Psychiatry, 59 (2), pp. 144-151.
5. Asahina M., Kikkawa Y., Suzuki A., Hattori T. (2003), “Cutaneous sympathetic function in patients with multiple system atrophy”. Clin Auton Res, 13 (2), pp. 91-5.
6. Bonuccelli U., Lucetti C., Del Dotto P., et al. (2003), “ORthostatic hypotension in de novo parkinson disease”. Arch Neurol, 60 (10), pp. 1400-1404.
7. Bordet R., Benhadjali J., Destee A., Hurtevent J. F., Bourriez J. L., et al. (1996), “Sympathetic skin response and R-R interval variability in multiple system atrophy and idiopathic Parkinson’s disease”. Mov Disord, 11 (3), pp. 268-72.
8. Chowdhury D., Patel N. (2006), “Approach to a case of autonomic peripheral neuropathy”. J Assoc Physicians India, 54, pp. 727-32.
9. Ewing D. J., Martyn C. N., Young R. J., Clarke B. F. (1985), “The value of cardiovascular autonomic function tests: 10 years experience in diabetes”. Diabetes Care, 8 (5), pp. 491-8.
10. Gilman S., Wenning G. K., Low P. A., Brooks D. J., Mathias C. J., et al. (2008), “Second consensus statement on the diagnosis of multiple system atrophy”. Neurology, 71 (9), pp. 670-6.
11. Jamora R. D., Gupta A., Tan A. K., Tan L. C. (2005), “Clinical characteristics of patients with multiple system atrophy in Singapore”. Ann Acad Med Singapore, 34 (9), pp. 553-7.
12. Kimber J., Mathias C. J., Lees A. J., Bleasdale-Barr K., Chang H. S., et al. (2000), “Physiological, pharmacological and neurohormonal assessment of autonomic function in progressive supranuclear palsy”. Brain, 123 ( Pt 7), pp. 1422-30.
13. Kimpinski K., Iodice V., Burton D. D., Camilleri M., Mullan B. P., et al. (2012), “The role of autonomic testing in the differentiation of Parkinson’s disease from multiple system atrophy”. J Neurol Sci, 317 (1-2), pp. 92-6.
14. Lipp A., Sandroni P., Ahlskog J. E., Fealey R. D., Kimpinski K., et al. (2009), “Prospective differentiation of multiple system atrophy from Parkinson disease, with and without autonomic failure”. Arch Neurol, 66 (6), pp. 742-50.
15. Low P. A., Tomalia V. A., Park K. J. (2013), “Autonomic function tests: some clinical applications”. J Clin Neurol, 9 (1), pp. 1-8.
16. Nagappan R., Arora S., Winter C. (2002), “Potential dangers of the Valsalva maneuver and adenosine in paroxysmal supraventricular tachycardia–beware preexcitation”. Crit Care Resusc, 4 (2), pp. 107-11.
17. Pepine C. J., Wiener L. (1979), “Effects of the Valsalva maneuver on myocardial ischemia in patients with coronary artery disease”. Circulation, 59 (6), pp. 1304-11.
18. Riley D. E., Chelimsky T. C. (2003), “Autonomic nervous system testing may not distinguish multiple system atrophy from Parkinson’s disease”. J Neurol Neurosurg Psychiatry, 74 (1), pp. 56-60.
19. Sandroni P., Ahlskog J. E., Fealey R. D., Low P. A. (1991), “Autonomic involvement in extrapyramidal and cerebellar disorders”. Clin Auton Res, 1 (2), pp. 147-55.
20. Tada M., Onodera O., Ozawa T., Piao Y. S., Kakita A., et al. (2007), “Early development of autonomic dysfunction may predict poor prognosis in patients with multiple system atrophy”. Arch Neurol, 64 (2), pp. 256-60.
21. Watanabe H., Saito Y., Terao S., Ando T., Kachi T., et al. (2002), “Progression and prognosis in multiple system atrophy: an analysis of 230 Japanese patients”. Brain, 125 (Pt 5), pp. 1070-83.