Chủ biên: Nguyễn Văn Tuận1, Võ Hồng Khôi 1 Thành viên: Lê Văn Tuấn 2, Nguyễn Hồng Quân3, Đinh Huỳnh Tố Hương4 Hoàng Tiến Trọng Nghĩa 5, Lê Văn Thủy 6, Hoàng Thị Thanh Thúy 7, Nguyễn Hữu Công 8 1 Trung tâm Thần kinh, Bệnh viện Bạch Mai 2 Trung tâm Thần kinh, Bệnh viện Tâm Anh,TP. Hồ Chí Minh 3 Khoa Thần kinh, Bệnh viện Trung ương Quân đội 108 4 Khoa Thần kinh, Bệnh viện Đại Học Y Dược TP. Hồ Chí Minh 5 Trung tâm Thần kinh, Bệnh viện Quân y 175 6 Bệnh viện Đai học Y Hà Nội 7 Bệnh viện Hữu Nghị 8 Bệnh viện Ngoại Thần kinh quốc tế
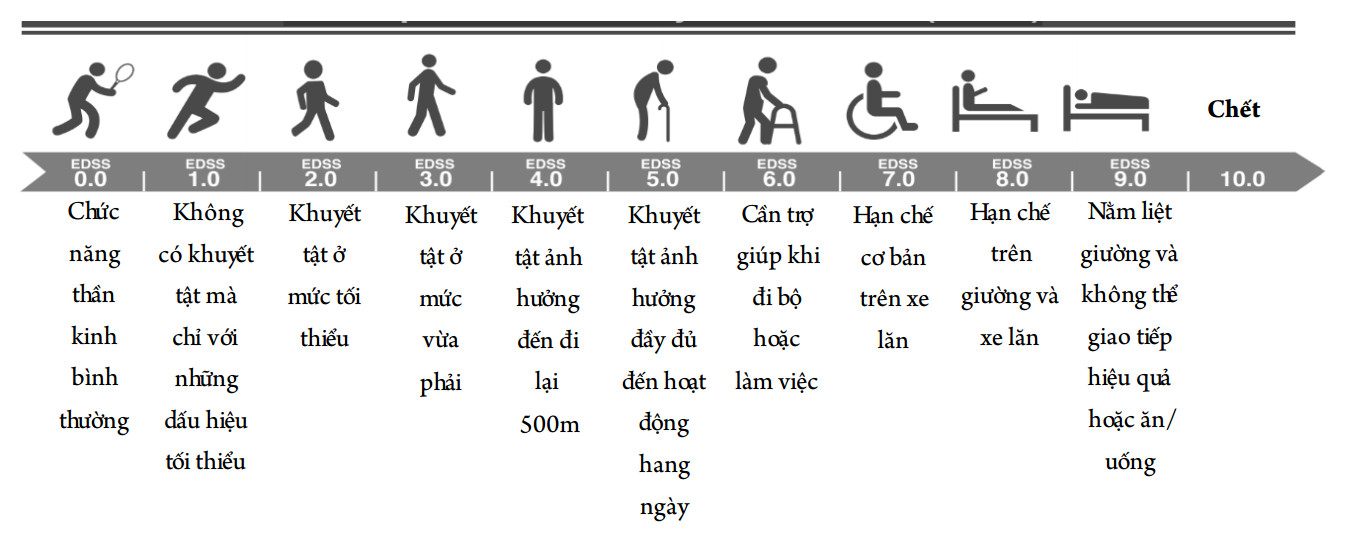
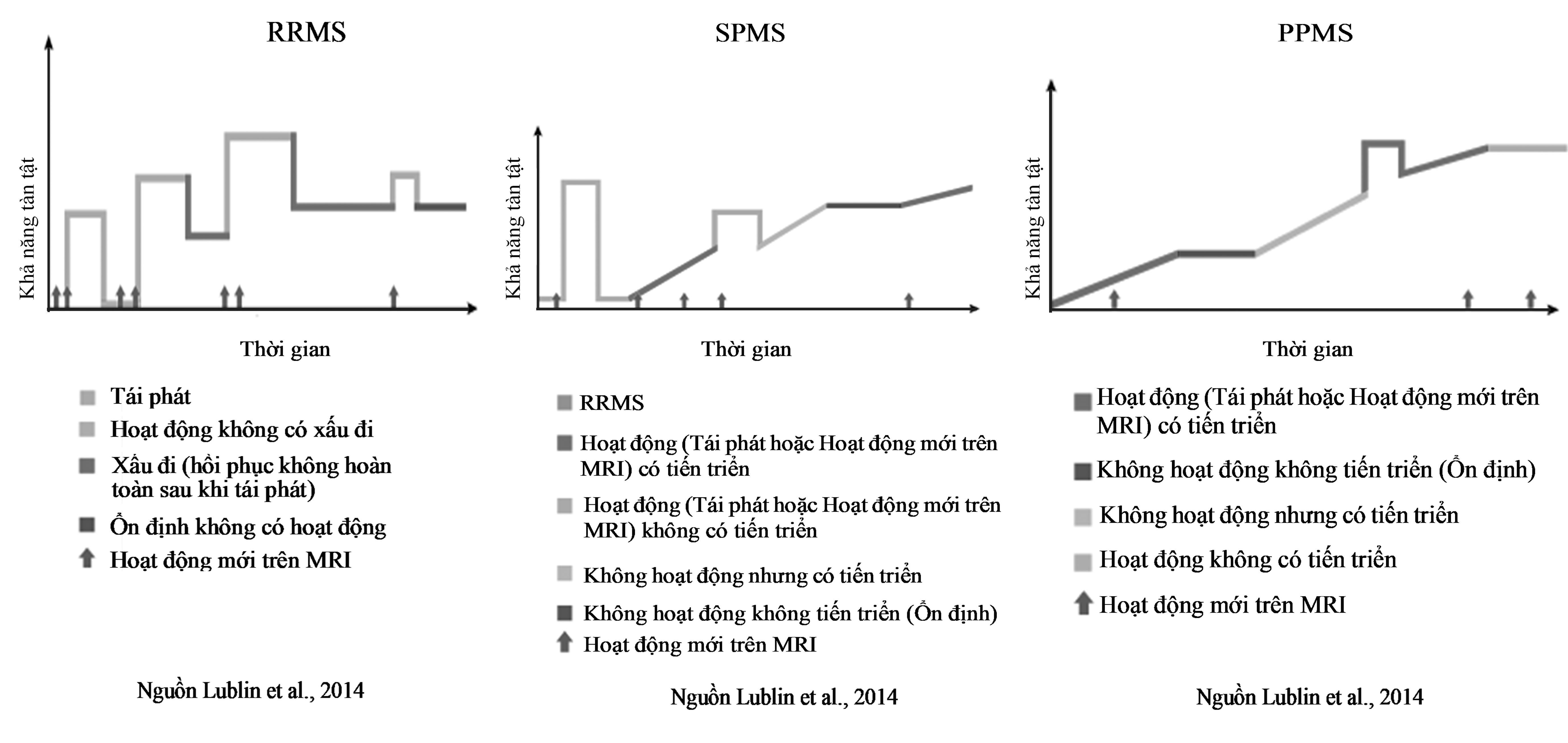
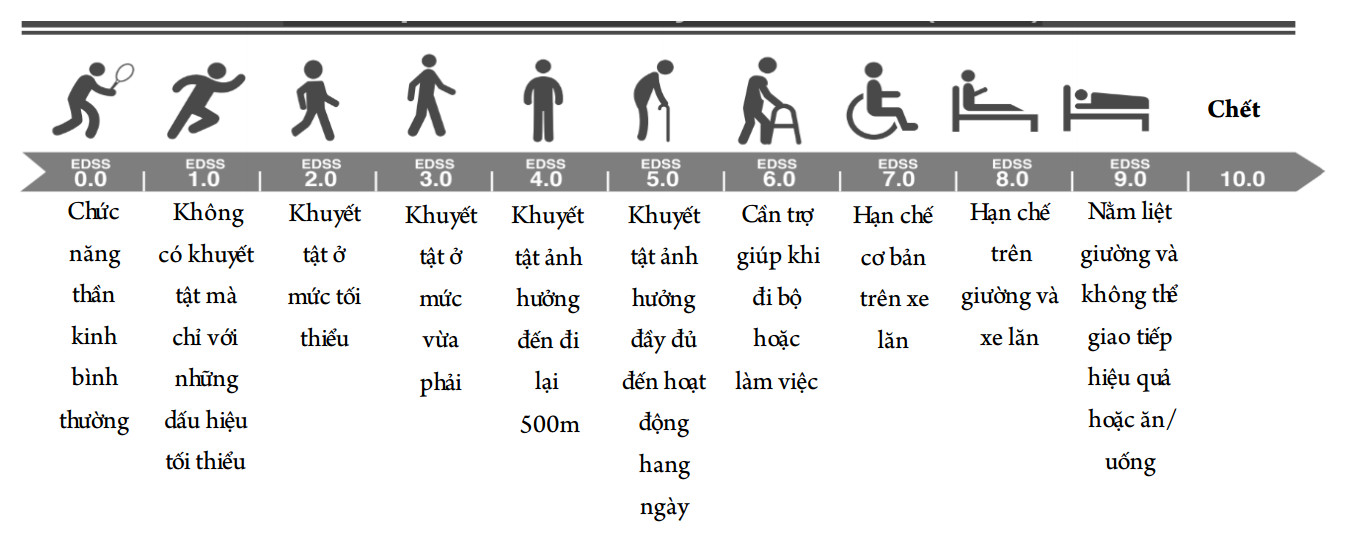
1. ĐẠI CƯƠNG 1.1. Mục đích của hướng dẫn điều trị Đối tượng: Người lớn từ 18 tuổi trở lên tại Việt Nam. Mục đích: Cải thiện chất lượng cuộc sống cho những người bệnh xơ cứng rải rác bằng cách thúc đẩy điều trị triệu chứng nhanh chóng và hiệu quả, điều trị tái phát và đánh giá toàn diện. 1.2. Định nghĩa Xơ cứng rải rác (multiple sclerosis-MS) là bệnh tự miễn của hệ thần kinh trung ương, đặc trưng bởi viêm mất myelin mạn tính, tăng sinh thần kinh đệm (tạo mảng hoặc sẹo) và mất neuron thần kinh, diễn biến có thể tái phát từng đợt hoặc tiến triển. Những mảng mất myelin thường phát triển ở những thời điểm khác nhau và ở những vị trí khác nhau của hệ thần kinh trung ương (rải rác theo không gian và thời gian). Các triệu chứng và dấu hiệu thần kinh là biểu hiện của những ổ tổn thương và sự lan rộng của những ổ mất myelin, xảy ra chủ yếu ở chất trắng của não, tủy, hoặc dây thần kinh thị giác. 1.3. Dịch tễ học Trên thế giới có khoảng 2,8 triệu người bị xơ cứng rải rác, với tỷ lệ mắc bệnh trung bình 35,9/100.000 dân, có phân bố địa lý không đều, gặp nhiều nhất ở châu Âu 133/100.000, châu Mỹ 112/100.000, tỉ lệ thấp hơn ở Đông Nam Á 9/100.000 và châu Phi 5/100.000 và khu vực Tây Thái Bình dương 5/100000 dân.1,2 Khởi phát bệnh thường ở lứa tuổi trung bình khoảng 32 (đa phần từ 20- 40 tuổi). Phụ nữ nhiều hơn hai lần so với nam giới. Căn nguyên gây bệnh còn chưa biết rõ, các tác giả đề cập đến các yếu tố phơi nhiễm môi trường xung quanh và gen mà nó ảnh hưởng lên tính nhạy cảm của cả hệ miễn dịch và cơ quan đích. 1.4. Giải phẫu bệnh Bệnh tự miễn dịch MS được đặc trưng bởi hai quá trình bệnh lý:3,4 + Có quá trình viêm: Hoạt hóa tế bào lympho T, mono bào, lympho B, gây mất myelin từng mảng và tổn thương sợi trục. + Đồng thời làm tăng sinh tế bào thần kinh đệm và thoái hóa thần kinh Cuối cùng gây teo não, teo tủy. Tổn thương nhu mô trong MS chỉ giới hạn ở hệ thần kinh trung ương (TKTW) mà không có tổn thương hệ thần kinh ngoại vi. 1.5. Một số khái niệm Xơ cứng rải rác (Multiple sclerosis) (Tiếng Anh), xơ cứng mảng (sclérose en plaques) (Tiếng Pháp): những mảng tổn thương mất myelin của hệ TKTW. Hội chứng lâm sàng đơn lẻ (CIS- Clinically Isolated Syndrome) là đợt đầu tiên xuất hiện triệu chứng lâm sàng gây nên bởi viêm mất myelin của hệ TKTW ảnh hưởng đến: dây thần kinh thị giác, thân não, tủy sống. CIS thường biểu hiện đợt đầu tiên của MS. Hội chứng hình ảnh học đơn lẻ (RIS-Radiologically Isolated Syndrome) bất thường trên hình ảnh học gợi ý viêm mất myelin nhưng không biểu hiện lâm sàng. RIS có thể tăng nghi ngờ MS tùy thuộc vào hình thái và vị trí của tổn thương trên cộng hưởng từ (MRI). RIS vẫn chưa được coi là một dưới nhóm của bệnh MS. Bệnh nhân MS đang tiến triển bị tái phát hoặc được phát hiện có tổn thương mới cấp tính trên MRI được coi là có MS "hoạt động". Thuật ngữ "Tiến triển" được dành để mô tả sự suy giảm thần kinh tích lũy độc lập với hoạt động của bệnh. Đợt cấp được xác định bằng tái phát trên lâm sàng và/hoặc thay đổi hình ảnh thần kinh (tổn thương ngấm thuốc đối quang từ hoặc tổn thương T2 mới/lan rộng trên MRI). Mỗi đợt, các triệu chứng phải kéo dài ít nhất 24 giờ và xảy ra thành các đợt riêng biệt cách nhau ít nhất 1 tháng, không có sốt, không có nhiễm trùng và loại trừ các bệnh khác. 1.6. Tiến triển bệnh Ủy ban Cố vấn Quốc tế về các thử nghiệm lâm sàng của MS năm 2013, xác định có 3 kiểu tiến triển bệnh MS:5,6 - Tái phát - thuyên giảm (relapsing-remitting MS- RRMS) - Tiến triển nguyên phát (Primary progressive MS -PPMS) - Tiến triển thứ phát (secondary progressive MS-SPMS).
Đo lường sự tiến triển: Tiến triển trong MS là thuật ngữ được sử dụng để xác định sự xấu dần mà không phải đợt cấp của các triệu chứng và dấu hiệu trong vòng 6-12 tháng. Sự tiến triển của bệnh MS có thể được theo dõi trên lâm sàng dựa vào thang điểm đánh giá mức độ tàn tật và suy giảm của MS (The Expanded Disability Status Scale-EDSS).6
2. TRIỆU CHỨNG LÂM SÀNG 2.1. Những triệu chứng và dấu hiệu ban đầu Những triệu chứng và dấu hiệu ban đầu ảnh hưởng đến những phần khác nhau của cơ thể có thế gợi ý MS. Thường gặp nhất là:7 Mất hoặc giảm thị lực ở 1 mắt, có thể kèm đau trong/ sau nhãn cầu tăng khi liếc mắt Nhìn đôi Rối loạn cảm giác hoặc dị cảm tay chân Yếu chi (tăng phản xạ gân xương, dấu hiệu Babinski) Thay đổi cảm giác hoặc cơn đau lan xuống lưng và đôi khi lan ra tứ chi khi cúi cổ về phía trước (dấu hiệu L’hermitte) Đau dây V Mất thăng bằng và chóng mặt, di chuyển khó khăn Rối loạn chức năng bàng quang, rối loạn chức năng tình dục, mệt mỏi 2.2. Một số lưu ý Tuổi khởi phát thường dưới 50 Có thể tiền sử có triệu chứng thần kinh trước đó Các triệu chứng phải kéo dài ít nhất 24 giờ và sau đó cải thiện Các đợt riêng biệt cách nhau ít nhất 1 tháng, Không có sốt, không có nhiễm trùng Loại trừ các bệnh khác. Người có triệu chứng nên được khám bởi bác sĩ chuyên khoa thần kinh để xác định bệnh.
3. CHẨN ĐOÁN XƠ CỨNG RẢI RÁC 3.1. Chẩn đoán xác định Chẩn đoán xác định đòi hỏi phải có bằng chứng khách quan tổn thương viêm mất myelin của hệ thần kinh trung ương và tổn thương có tính chất rải rác theo không gian và thời gian và loại trừ các bệnh khác.8,9 - Tiêu chuẩn McDonald năm 2017 chẩn đoán xơ cứng rải rác.8
| Số đợt lâm sàng | Số tổn thương lâm sàng khách quan | Dữ kiện bổ sung cần cho chẩn đoán xơ cứng rải rác |
| 2 | 2 | Không* |
| 2 | 1 (và trong tiền sử có bằng chứng rõ ràng của một đợt lâm sàng trước đó liên quan đến tổn thương tại một vị trí giải phẫu khác) | Không* |
| 2 | 1 | Rải rác theo không gian được chứng minh trên MRI hoặc chờ thêm 1 đợt lâm sàng liên quan đến vị trí khác của hệ thần kinh trung ương. |
| 1 | 2 | Rải rác theo thời gian được chứng minh trên MRI hoặc có thêm 1 đợt lâm sàng hoặc dịch não tủy có dải đơn dòng đặc hiệu (Oligoclonal bands). |
| 1 | 1 | Rải rác theo không gian được chứng minh trên MRI hoặc có thêm 1 đợt lâm sàng liên quan đến vị trí khác của hệ thần kinh trung ương Và Rải rác theo thời gian được chứng minh trên MRI hoặc có thêm 1 đợt lâm sàng hoặc dịch não tủy có dải đơn dòng đặc hiệu (Oligoclonal bands). |
| 0 Tiến triển TK âm ỉ từ khi khởi phát | Tiến triển khuyết tật thần kinh 1 năm (xác định qua hồi cứu hoặc tiến cứu) không phụ thuộc vào tái phát lâm sàng. Và ít nhất 2/3 tiêu chuẩn sau: * ≥ 1 tổn thương tăng tín hiệu T2 ở ≥ 1 vùng của não đặc trưng của MS: cạnh não thất, cận vỏ não hoặc vỏ não, hoặc dưới lều. * 2 tổn thương tăng tín hiệu T2 trên MRI tủy sống * Có dải đơn dòng đặc hiệu (Oligoclonal bands). | |
| *Không cần các dữ kiện bổ sung để chứng minh rải rác theo thời gian và không gian. Tuy nhiên, trừ trường hợp không có sẵn tại cơ sở y tế, MRI sọ não nên được thực hiện trên tất cả bệnh nhân mà chẩn đoán xơ cứng rải rác đang được nghĩ tới. | ||
- Tiêu chuẩn rải rác trong không gian và thời gian trên MRI: Rải rác trong không gian bởi có ít nhất một tổn thương ở ít nhất 2 trong 4 vị trí điển hình của MS (cạnh não thất, cận vỏ hoặc vỏ não, dưới lều, tủy sống) Rải rác theo thời gian là có xuất hiện đồng thời các tổn thương tăng tín hiệu thuốc đối quang từ và tổn thương không tăng tín hiệu ở bất kỳ thời điểm nào; hoặc có tổn thương mới trên T2 hoặc tổn thương ngấm thuốc đối quang từ mới trên cộng hưởng từ ở lần chụp sau so với lần chụp trước. - Mỗi tổn thương lâm sàng khách quan tương ứng với mỗi vị trí giải phẫu đặc trưng của xơ cứng rải rác trên cộng hưởng từ: dây thần kinh thị giác, tủy sống hoặc dưới lều (thân não, tiểu não), hoặc não (cận vỏ hoặc vỏ não, cạnh não thất). Liên quan tới bằng chứng tổn thương lâm sàng khách quan (tình trạng của đợt cấp hiện tại hoặc trong tiền sử), là bất thường tìm thấy khi khám lâm sàng thần kinh, hình ảnh học (MRI hoặc chụp quang học mắt OCT) hoặc điện sinh lý thần kinh (điện thế gợi thị giác) phù hợp với vị trí giải phẫu gợi nên bởi các triệu chứng khách quan của người bệnh. 3.2. Chẩn đoán phân biệt Có rất nhiều bệnh cần phân biệt với bệnh xơ cứng rải rác:1 - Nhiễm khuẩn hệ thần kinh: bệnh Lyme, giang mai, HIV, … - Tình trạng viêm hệ TKTW: sarcoidosis, lupus, Sjӧgren, hội chứng kháng phospholipid, viêm mạch (vasculitis), viêm não tủy rải rác cấp tính (ADEM), Phổ bệnh viêm tủy thị thần kinh (NMOSD), MOGAD… - Bệnh lý mạch máu của hệ TKTW: nhồi máu não, bệnh gây nên do tăng huyết áp và đái tháo đường, viêm mạch, CADASIL, MELAS. - Rối loạn về di truyền: leukodystrophy, bệnh tủy do di truyền, bệnh ty lạp thể. - Những khối choán chỗ nội sọ não hoặc chèn ép tủy: khối u, thoát vị đĩa đệm, dị dạng Chiari, viêm cột sống dính khớp vùng cổ. - Thiếu vitamin B12…
4. CẬN LÂM SÀNG 4.1. Chụp cộng hưởng từ - Chụp cộng hưởng từ não, tủy và dây thần kinh thị giác để đánh giá những tổn thương của MS có tính chất rải rác trong không gian và thời gian, đồng thời loại trừ những bệnh khác: + Những tổn thương ở những vị trí khác nhau (rải rác trong không gian), các vị trí đặc trưng của MS: cạnh não thất, cận vỏ hoặc vỏ não, dưới lều (thân não, tiểu não), tủy sống (tổn thương thường ở vùng ngoại vi của tủy, kích thước thường dưới 3 đốt sống), dây thần kinh thị giác. Ngoài ra có thể đánh giá những tổn thương ở thể chai, những tổn thương tăng tín hiệu trên T2 và trên FLAIR đi vuông góc và tiếp giáp với màng não thất (“bàn tay của Dawson”). Những tổn thương mất myelin của MS thường có hình tròn hoặc hình oval, với kích thước trên T2 ít nhất từ 3 mm hoặc tổn thương có hình chữ U ở vùng cận vỏ não. + Tổn thương ở những giai đoạn khác nhau có thể biểu hiện trên một lần chụp như tổn thương tăng tín hiệu thuốc đối quang từ và tổn thương tăng tín hiệu trên T2 nhưng không tăng tín hiệu thuốc đối quang từ ở bất kỳ thời điểm nào; hoặc có tổn thương mới trên T2 hoặc tổn thương ngấm thuốc đối quang từ trên cộng hưởng từ ở lần chụp sau so với lần chụp trước (rải rác theo thời gian). Những tổn thương cũ có thể tạo nên những “lỗ đen” (black holes) giảm tín hiệu trên MRI ở xung T1 ở giai đoạn muộn. MRI não và tủy sống vẫn là xét nghiệm cận lâm sàng hữu ích nhất để hỗ trợ chẩn đoán bệnh xơ cứng rải rác và có thể thay thế cho các kết quả lâm sàng trong việc xác định tính chất rải rác trong không gian hoặc rải rác theo thời gian ở những bệnh nhân có hội chứng lâm sàng đơn lẻ điển hình. Chụp MRI dây thần kinh thị giác có thể phát hiện tổn thương dây thần kinh thị giác như tăng kích thước, tăng tín hiệu T2 dây thần kinh thị giác, tổn thương giao thoa thị giác và độ dài tổn thương ngấm thuốc đối quang từ của dây thần kinh thị giác, ngoài ra có thể đánh giá trong hốc mắt, tuyến lệ, gai thị. - Ngoài ra có thể chụp quang học mắt OCT (Optical Coherence Tomography) có thể hỗ trợ phân tích sự thoái hóa thần kinh trong MS bằng cách ghi lại sự mỏng đi của lớp sợi thần kinh võng mạc. 4.2. Dịch não tủy Dịch não tủy trong giai đoạn cấp có thể thấy: - Tăng nhẹ protein dưới 1g/l (gặp 40% các trường hợp). - Tăng bạch cầu lympho vừa phải < 50 bạch cầu/mm³. - Tăng gammaglobulin (Tăng IgG) thấy 75% các trường hợp. - Dải đơn dòng (oligoclonal bands- OCBs) dương tính khoảng 85%. 4.3. Xét nghiệm máu Không có xét nghiệm máu đặc hiệu nào cho chẩn đoán MS, tuy nhiên có 1 số xét nghiệm tìm bệnh khác gây tổn thương giống MS như bệnh Lyme, nhóm bệnh mạch máu- collagen, HIV, một số rối loạn di truyền hiếm gặp, và để loại trừ bệnh khác. Xét nghiệm kháng thể kháng Aquaporin4 - IgG (dương tính trong phổ bệnh viêm tủy thị thần kinh). Xét nghiệm kháng thể MOG (myelin oligodendrocyte glycoprotein) 4.4. Điện thế gợi Ghi điện thế gợi thị giác, vận động, cảm giác thân thể, thính giác thân não có thể cho phép xác định tổn thương thần kinh dưới lâm sàng nhưng thường không đặc hiệu và không hằng định.
5. ĐIỀU TRỊ 5.1. Nguyên tắc - Điều trị đợt cấp (MS và CIS) - Điều trị triệu chứng - Điều trị theo cơ chế bệnh sinh (DMT) 5.2. Điều trị đợt cấp tính - Methylprednisolone liều cao (0,5g đến 1g/ ngày) truyền tĩnh mạch trong 3 đến 5 ngày.9 - Điều trị bậc 2 cho nhưng bệnh nhân kháng thuốc, hoặc đáp ứng kém với glucocorticoid gồm: Thay huyết tương, Globulin miễn dịch và adrenocorticotropic hormone (ACTH).1,9 + Thay huyết tương dành cho những trường hợp triệu chứng nghiêm trọng, không đáp ứng với glucocorticoid. Số lần lọc huyết tương 5 lần, nếu cải thiện có thể thêm 2-5 lần nữa. + Truyền tĩnh mạch Globulin miễn dịch chưa được chấp thuận trong chỉ định này nhưng một số trường hợp không đáp ứng với steroid, nhưng đáng chú ý đây là điều trị ưu tiên cho bệnh nhân sau sinh. + ACTH (nếu có) là một lựa chọn khác nhưng hiếm khi được sử dụng vì chi phí cao và lợi thế không chắc chắn so với glucocorticoid, ở một số bệnh nhân tiếp cận đường tĩnh mạch khó hoặc không dung nạp với corticosteroid đường uống. Thông tin về điều trị đợt cấp với steroid: • Thảo luận về lợi ích và nguy cơ của steroid ở người bệnh MS, có tính đến ảnh hưởng của đợt tái phát đến khả năng thực hiện các công việc thông thường và sức khỏe của họ. • Giải thích về các biến chứng tiềm ẩn của steroid liều cao (ví dụ tác dụng tạm thời ảnh hưởng đến sức khỏe tâm thần: mất ngủ, trầm cảm, lú lẫn và kích thích) và xấu đi việc kiểm soát đường máu ở người bệnh đái đường. • Cung cấp cho người MS và các thành viên gia đình của họ hoặc người chăm sóc họ (nếu thích hợp) thông tin mà họ có thể biết về tác dụng phụ của steroid liều cao ở dạng phù hợp với họ. • Phải thông báo về tình trạng đợt tái phát cho các bác sĩ chuyên ngành liên quan tham gia chăm sóc bệnh nhân. 5.3. Điều trị triệu chứng Trong quá trình tiến triển của bệnh, các triệu chứng xuất hiện có khuynh hướng tăng dần. Bệnh MS có các triệu chứng đa dạng, gây ra thiếu sót chức năng thần kinh và gây tàn tật. Vậy phải điều trị cả thuốc và phục hồi chức năng thần kinh.10 5.3.1. Co cứng - Cơ cứng là triệu chứng thường gặp ở bệnh nhân mắc MS, cần được điều trị tốt bằng phối hợp nhiều chuyên khoa (thần kinh, phục hồi chức năng, vậy lý trị liệu, điều dưỡng chuyên khoa) để tránh biến chứng như co rút gân, co rút và biến dạng phần mềm làm tăng tình trạng tàn phế. - Việc điều trị và quản lý bệnh nhân co cứng do MS cần thực hiện theo các bước: (1) Đánh giá các cơ bị ảnh hưởng một cách toàn diện, xem xét tình trạng co cứng là cục bộ hay toàn thể. (2) Đánh giá các triệu chứng kèm theo của co cứng, hay gặp là các cơn co thắt (thường gây đau nhưng co thể bị triệu chứng co cứng che lấp). (3) Xác định và điều trị cả các yếu tố khởi phát co cứng (rối loạn tiểu tiện, tư thế, loét tì đè). (4) Lên kế hoạch vật lý trị liệu và can thiệp điều dưỡng. (5) Tối ưu hoá thuốc điều trị (dùng thuốc đơn độc hay phối hợp vật lý trị liệu).
| Các phương pháp điều trị co cứng cục bộ và toàn thể trong xơ cứng rải rác | |
| Co cứng cục bộ | Co cứng toàn thể |
| Cân nhắc vật lý trị liệu, các phương pháp kéo dãn | Thuốc đường uống |
| Cân nhắc dùng dụng cụ dạng nẹp | Các can thiệp trong ống sống (Bơm Baclofen) Hiện chưa khả dụng ở Việt Nam |
| Botulinum Toxin | Cân nhắc phục hồi chức năng |
- Các thuốc sử dụng để làm giảm triệu chứng co cứng có nhiều loại thuộc nhiều nhóm, trong thực hành, bắt đầu từ một thuốc thuộc một nhóm trước sau đó tăng dần liều, nếu không thể tăng thêm liều và kém hiệu quả có thể cân nhắc kết hợp thuốc nhiều nhóm với nhau. Đôi khi có thể kết hợp phương pháp điều trị toàn thân (thuốc uống) với điều trị tại chỗ (tiêm Botulinum Toxin).11
| Thuốc | Cơ chế | Liều | Tác dụng phụ |
| Baclofen | Ức chế hoạt động tự động tuỷ | Khởi đầu từ 5mg x 3 lần/ngày tới tối đa 40 mg x 3 lần /ngày | An thần, ngủ gà, yếu cơ, dị cảm, nôn, khô miệng |
| Tizanidine | Giảm giải phóng chất dẫn truyền kích thích thần kinh ở tuỷ (Glutamate và aspartate) | Khởi đầu 2mg x 3 lần /ngày tới 8 mg x 3 lần /ngày (tối đa 12 mg x 3 lần /ngày) | Mệt mỏi, ngủ gà, choáng váng, khô miệng, hạ huyết áp tư thế, tăng men gan. |
| Clonazepam | Tăng cung phản xạ ức chế của tuỷ | 0,25 mg tới 2 mg một lần /ngày | Ngủ gà, mệt mỏi, an thần, giảm tập trung, phụ thuộc thuốc, gây hội chứng cai nếu ngừng đột ngột |
| Gabapentin | Giảm giải phóng Glutamate | 300 mg một lần/ ngày tăng tới 300 mg 3 lần/ngày, tối đa 1200 mg x 3 lần/ ngày | Ngủ gà, choáng váng, rối loạn tiêu hoá. |
| Dantrolen | Giảm lực co từ hệ cơ vân | 75 mg x 3 lần / ngà (tối đa 100 mg x 4 lần /ngày) | Ngủ gà, mệt mỏi, nôn, tiêu chảy, mệt mỏi, dị cảm, yếu cơ, độc. cho gan |
5.3.2. Đau - Các cơn đau kịch phát trong MS - Đau dây V: tương tự với điều trị đau dây V tiên phát carbamazepine là lựa chọn đầu tay, song cần chú ý nguy cơ dị ứng thuốc nặng. Các thuốc khác có thể cân nhắc nếu dị ứng hoặc không dung nạp như Gabapentine, Pregabaline. - Dấu hiệu Lhernmitte: Pregabaline, Gabapentine hoặc Carbamazepin. - Co thắt cơ hay triệu chứng kiểu đè nén, ép chặt ở một phần cơ thể thường ở bụng và ngực ("MS hug"): Các thuốc cân nhắc gồm amitryptilin, gabapentine, pregabaline, carbamazepine. - Các cơn đau co thắt tăng trương lực của một nhóm cơ ở chi, thân mình hoặc đôi khi ở mặt: cân nhắc các thuốc chống động kinh nhóm Carbamazepine hoặc Valproat acid. - Triệu chứng đau dai dẳng trong MS. - Đau dai dẳng nguồn gốc trung ương là triệu chứng quan trọng gây tàn phế cho bệnh nhân MS. - Thuốc có thể cân nhắc là nhóm chống trầm cảm 3 vòng (Amitryptilin), thuốc ức chế tái hấp thu Serotonin hoặc Norepinephrine (duloxetine, venlafaxine) và các thuốc chống động kinh (gabapentine, pregabaline, lamotrigine, levetiracetam). - Các phương pháp không dùng thuốc có thể được cân nhắc: • Phương pháp không xâm lấn như kích thích từ trường xuyên sọ. • Phương pháp xâm lấn: khi thất bại với các phương pháp khác (kích thích thần kinh qua da (TENS)). 5.3.3. Điều trị trầm cảm ở bệnh nhân MS - Nếu đi kèm triệu chứng đau thần kinh: các thuốc nhóm duloxentin, Venlafaxin. - Nếu triệu chứng lo âu nổi trội: ưu tiên dùng SSRIs như Escitalopram, sertraline. - Nếu kèm theo ngủ ngày nhiều: có thể ưu tiên venlafaxine. 5.3.4. Tình trạng mệt mỏi ở bệnh nhân MS - Phối hợp can thiệp dùng thuốc và không dùng thuốc (hoạt động thể lực vừa phải, làm mát tích cực (áo làm mát, miếng làm mát), liệu pháp tâm lý hành vi và giáo dục người bệnh. - Dùng thuốc có thể cân nhắc:
| Thuốc | Cơ chế | Liều | Tác dụng phụ |
| Amantadine | Tác động trên hệ Cholinergic và Glutamanergic của hệ TKTW | 100mg x 2 lần /ngày, tối đa 600 mg /ngày | Chán ăn, nôn, mất ngủ, ảo thị, nhìn nhoè hình, khó chịu dạ dày - ruột, ban dạng lưới, phù ngoại vi, khô miệng, khó tiểu |
| Modafinil | Thuốc kích thần | 100-300 mg (tối đa 400 mg /ngày) | Bồn chồn, mất ngủ, lo lắng, nhịp nhanh, đau đầu, tăng nguy cơ co giật, ảo thị. |
| Amynopyridine | Ức chế kênh Kali, kéo dài thời gian pha điện thế hoạt động và tăng giải phóng chất dẫn truyền thần kinh | 5mg 1 lần / ngày tăng tới 10-20 mg x 3 lần / ngày | Dị cảm, choáng váng, co giật, lo lắng, mất ngủ, đau đầu, run |
| Pemoline | Chất kích thần | 20 mg tới tối đa 60 mg | Mất ngủ, kích thích, chán ăn, sút cân, nhịp nhanh, tăng nguy cơ co giật |
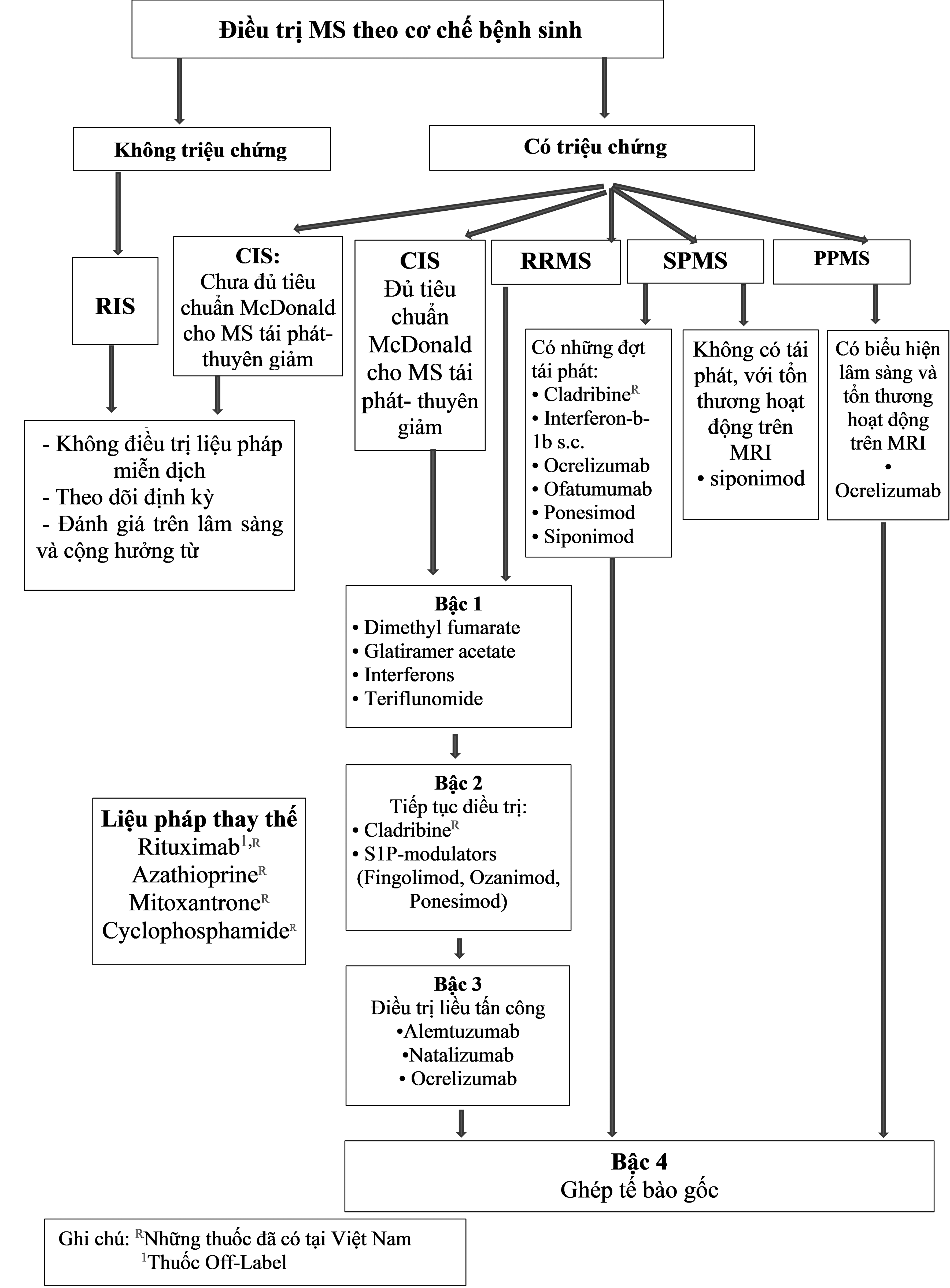
5.3.5. Rối loạn chức năng bàng quang - Rối loạn chức năng bàng quang rất hay gặp tới 75 % bệnh nhân MS. Hay đi kèm với các triệu chứng khác của tổn thương tháp như co cứng, yếu cơ; triệu chứng cảm giác như đau nguồn gốc tuỷ sống, rối loạn chức năng tình dục và ruột. - Triệu chứng đa dạng do hậu quả của tăng hoạt động bàng quang (tiểu gấp, tiểu nhiều lần, tiểu không thể kìm) và bàng quang hoạt động mất hiệu quả (mất khả năng làm trống bàng quang, tồn dư nước tiểu..). Có thể đi kèm theo hiện tượng mất đồng bộ của cơ Detrusor và cơ thắt cổ bàng quang (co thắt cùng lúc dẫn tới tiểu ngập ngừng, dòng tiểu gián đoạn và không thể làm trống hoàn toàn bàng quang). - Các phương pháp chăm sóc chung: Duy trì lượng nước uống (1-2l/ngày). Sử dụng các bài tập làm mạnh cơ vùng sàn chậu kèm hoặc không kèm phản hồi từ điện cơ cho các bệnh nhân ở mức độ tàn tật vừa phải. - Quản lý tình huống bàng quang hoạt động không hiệu quả. + Tự đặt sonde tiểu ngắt quãng: Đây là phương pháp điều trị chính cho các trường hợp không thể làm trống bàng quang hoàn toàn với lượng nước tiểu tồn dư > 100mL trở lên. Bệnh nhân cần được hướng dẫn bởi nhân viên có kinh nghiệm và giám sát để đảm bảo tự làm được một cách vô khuẩn. + Thuốc chẹn Alpha có thể được cân nhắc. + Đặt sonde kéo dài: Là phương pháp được áp dụng nếu thất bài với các phương pháp điều trị khác. Mở thông bàng quang trên xương mu nên được dùng thay cho đặt sonde niệu đạo. - Quản lý tình huống bàng quang tăng hoạt. + Thuốc kháng Muscarinic: Có thể sử dụng Oxybutynin với liều thấp và tăng liều chậm. Thận trọng với người lớn tuổi có suy giảm nhận thức. + Tiêm Botulinum toxin: Phối hợp với bác sĩ chuyên khoa ngoại tiết niệu có kinh nghiệm để tiêm thuốc vào vùng cơ Detrusor tăng hoạt dưới hướng dẫn của nội soi qua đường niệu đạo.11 + Desmopressin: cân nhắc cho các trường hợp bàng quang tăng hoạt kèm tiểu đêm nhiều lần. + Các phương pháp khác: thuốc chống trầm cảm loại SSRIs như Duloxetin. 5.3.6. Điều trị phục hồi chức năng (PHCN) PHCN tổng quát: Nhằm giảm thiểu tình trạng khuyết tật và tàn tật mà người bệnh phải trải qua. PHCN liên quan đến các can thiệp đa ngành: là sự phối hợp của 2 hoặc nhiều chuyên ngành (vật lý trị liệu, trị liệu nghề nghiệp, công tác xã hội, tâm lý học, điều dưỡng và các chuyên ngành khác) dưới sự giám sát của y tế (bác sĩ thần kinh và bác sĩ PHCN), nó được thiết kế lấy BN làm trung tâm, dựa trên thời gian và định hướng theo chức năng. Có đến 79% BN bị MS mất khả năng vận động. Trong vòng 10 năm kể từ khi được chẩn đoán 38% BN sẽ cần dụng cụ hỗ trợ và tỉ lệ này tăng lên 83% sau 30 năm. MS liên quan đến giảm hoạt động thể chất do bản thân căn bệnh này và hoặc do lối sống ít vận động, dẫn đến tăng tỷ lệ loãng xương, trầm cảm, mệt mỏi, mất sức mạnh cơ bắp, và tử vong do các bệnh tim mạch. Vật lý trị liệu nhằm mục đích cải thiện chức năng vận động, thăng bằng và dáng đi, và làm giảm tình trạng co cứng qua bài tập thụ động và chủ động: rèn luyên sức đối kháng, sức bền, và luyện tập sự kết hợp. PHCN dựa trên cải thiện sức cơ, khả năng chịu đựng và các hoạt động liên quan đến vận động ở mức vừa phải. Cả liệu pháp tập thể dục và liệu pháp tại nhà đều giúp cải thiện một số chức năng so với không tập thể dục ở BN MS. Chỉnh hình dáng đi do robot điều khiển cải thiện đáng kể sức bền khi đi bộ và sức mạnh đầu gối so với việc tập đi bộ thông thường ở BN MS bị khuyết tật nghiêm trọng (EDSS 6,0-7.5). Trị liệu nghề nghiệp: phục hồi và duy trì sự độc lập về chức năng điều chỉnh môi trường và sử dụng các thiết bị hỗ trợ. + MS gặp những hạn chế về khả năng thực hiện nhiều hoạt động cần thiết để sống độc lập về cá nhân, gia đình và cộng đồng. + Chức năng cánh tay hoặc chi trên là quan trọng để thực hiện hoạt động cần thiết để sống độc lập, đòi hỏi sự phối hợp vận động, sự khéo léo, và sự phối hợp chính xác giữa 2 tay. 5.4. Điều trị theo cơ chế bệnh sinh Điều trị MS theo cơ chế bệnh sinh9,12-32 nên được bắt đầu sớm với mục tiêu làm: - Giảm nguy cơ tái phát. - Giảm hoạt động bệnh lý, bảo tồn nhu mô não. - Hạn chế sự suy giảm nhận thức và tiến triến của tình trạng khuyết tật. Chọn lựa thuốc và thời gian điều trị: có thể phân thành 3 nhóm thuốc chính: + Nhóm thứ nhất: INF-beta, dimethyl fumarate, glatiramer axetat, và teriflunomide. + Nhóm thứ 2: Cladribine, fingolimod, ozanimod và + Nhóm thứ 3: Alemtuzumab, kháng thể kháng CD20: ocrelizumab, rituximab và natalizumab. Việc lựa chọn các thuốc dựa theo cơ chế bệnh sinh tùy thuộc vào từng bệnh nhân, dựa trên sự hoạt động của bệnh, tần suất tái phát và mức độ nghiêm trọng bệnh, đáp ứng với điều trị tái phát, tiến triển của bệnh và kết quả chụp cộng hưởng từ và theo nguyện vọng của bệnh nhân.
Phân bậc điều trị xơ cứng rải rác ở trên dựa theo hiệu quả điều trị của các thuốc tác động vào cơ chế bệnh sinh. Việc điều trị thực tế cần cân nhắc giữa tính hiệu quả, khả năng chấp nhận nguy cơ tác dụng phụ, cơ địa (ví dụ phụ nữ, nhu cầu có thai, cho con bú…), cũng như nguyện vọng của bệnh nhân. Liệu pháp thay thế gồm những thuốc có sẵn tại Việt Nam có thể được chọn lựa sử dụng khi các thuốc điều trị theo cơ chế bệnh sinh không có sẵn, tuy nhiên khi sử dụng phải tính đến giữa lợi ích và nguy cơ rủi ro cho người bệnh. Hiện nay, không có đủ bằng chứng về methotrexate, mycophenolate mofetil, azathioprine, cyclophosphamide như là điều trị duy trì để ngăn ngừa tái phát và tiến triển khuyết tật trong MS, tuy nhiên có thể sử dụng các thuốc này khi tất cả thuốc điều hòa miễn dịch khác không khả dụng. Vitamin D mặc dù không được chấp thuận như thuốc điều trị MS, tuy nhiên có thể khuyến cáo điều trị bổ sung cho người bệnh MS. Thay đổi trong điều trị cần được xem xét nếu:25 - Tần suất tái phát tăng - Phương pháp điều trị được coi là không phù hợp với bệnh nhân - Tình trạng thần kinh xấu đi kéo dài được quan sát thấy trong ≥2 lần kiểm tra liên tiếp (≥1 điểm EDSS) với khoảng thời gian 6 tháng giữa hai lần khám. - Đánh giá MRI được thực hiện trong 6 - 12 tháng đầu điều trị cho thấy có ≥1 tổn thương mới ngấm thuốc đối quang từ/và ≥2 tổn thương T2 mới hoặc lan rộng. Cần loại trừ giả tái phát và không tuân thủ trước khi chẩn đoán điều trị thất bại. Trong trường hợp không có hoạt động lâm sàng nhưng khi có hoạt động MRI, cần theo dõi lâm sàng chặt chẽ vì sự gia tăng tái phát hoặc điểm khuyết tật có thể cho thấy cần phải thay đổi liệu pháp điều trị. Đối với khu vực có nguồn lực hạn chế, Liên đoàn MS quốc tế (MSIF) đưa ra 2 khuyến cáo: bảng thuốc thiết yếu điều trị MS (MSIF Essential Medicines panel - MEMP) và thuốc điều trị MS ngoài hướng dẫn (MSIF Off-label Treatment - MOLT).31,32
| Danh mục thuốc thiết yếu điều trị MS | ||
| Alemtuzumab Azathioprine Cladribine Cyclophosphamide Daclizumab Dimethyl fumarate Diroximel fumarate Fingolimod Fludarabine Glatiramer acetate | Immunoglobulin Interferon beta – 1a Interferon beta – 1b Laquinimod Leflunomide Methotrexate Minocycline Mitoxantrone Monomethyl fumarate Mycophenolate mofetill | Natalizumab Ocrelizumab Ofatumumab Ozanimod PEG Interferon beta – 1a Ponesimod Rituximab Siponimod Steroid Teriflunomide |
Khuyến cáo MEMP32
| MS tái phát | MS tiến triển (SPMS) |
| Ủng hộ Claribine DMF Fingolimod Ocrelizumab Interferon beta – 1b Interferon beta – 1a Glatirarmer acetate | Ủng hộ Rituximab Glatirarmer acetate Ocrelizumab Interferon beta – 1a Fingolimod Interferon beta – 1b |
| Cân nhắc tùy trường hợp Natalizumab Alemtuzumab | Có thể thay thế nếu các thuốc khác không khả dụng Azathioprine Methotrexate |
| Không ủng hộ Mitoxantrone | Cân nhắc tùy trường hợp Siponimod Natalizumab Immunoglobulin |
Khuyến cáo MOLT
| MS tái phát | MS tiến triển (SPMS) |
| Ủng hộ Rituximab | Ủng hộ Rituximab |
| Có thể thay thế nếu các thuốc khác không khả dụng Azathioprine | Không thực hiện Azathioprine |
| HƯỚNG DẪN SỬ DỤNG THUỐC | ||
| GLATIRAMERE ACETATE | Chỉ định | MS thể tái phát – thuyên giảm - Từ 12 tuổi đối với COPAXONE® 20mg - Từ 18 tuổi đối với COPAXONE® 40mg |
| Liều | - 1 mũi tiêm dưới da (TDD) 40 mg glatiramer acetate 3 lần một tuần, cách nhau ít nhất 48 giờ. - Hoặc 1 mũi tiêm dưới da 20 mg glatiramer acetate mỗi ngày một lần | |
| Chống chỉ định chính | Không | |
| Đánh giá trước điều trị cụ thể | Không | |
| Theo dõi cụ thể | Không | |
| Mang thai và cho con bú | - Trong quá trình điều trị Glatiramer Acetate nếu chẩn đoán có thai vẫn có thể tiếp tục sử dụng nếu tiến triển của bệnh yêu cầu. - Có thể cho con bú ở những bệnh nhân được điều trị bằng Glatiramer Acetate. | |
| Chuyển đổi thuốc | Chuyển đổi Glatiramer Acetate sang phương pháp điều trị khác: - Dù điều trị nền là gì: Không cần trì hoãn nếu đáp ứng bilan trước điều trị bình thường. Chuyển sang Glatiramer Acetate - Dù điều trị nền là gì: Không cần trì hoãn nếu đáp ứng bilan trước điều trị bình thường. | |
| Tiêm chủng vacxin | - Tiêm chủng với lịch cộng đồng chung - Không có chống chỉ định với vắc-xin sống. | |
| INTERFERON β | Chỉ định | - RRMS từ 12 tuổi (trừ Plégridy® từ 18 tuổi) - SPMS có đợt tái phát thêm (Betaferon®, Rebif ®) |
| Liều | - AVONEX® 30 mg 1 lần tiêm bắp (TB)/tuần - BETAFERON® hoặc EXTAVIA® 250 mg TDD mỗi 2 ngày - PLEGRIDY® 125 mg TDD hoặc TB mỗi 2 tuần - REBIF ® 44 mg TDD X 3 mỗi tuần | |
| Chống chỉ định chính | - Viêm gan chưa được kiểm soát. - Hội chứng trầm cảm nặng và hoạt động. - Rối loạn chức năng tuyến giáp nặng | |
| Đánh giá trước điều trị cụ thể | - CTM, ALT, AST, TSH, urê, creatinine. | |
| Theo dõi cụ thể | - CTM, ALT, AST, urê, creatinine lúc 1, 3 và 6 tháng và sau đó mỗi năm. | |
| Mang thai và cho con bú | - Trong quá trình điều trị interferon β nếu chẩn đoán có thai vẫn có thể tiếp tục sử dụng nếu tiến triển của bệnh yêu cầu. - Có thể cho con bú ở những bệnh nhân được điều trị bằng Interferon β. | |
| Chuyển đổi thuốc | Chuyển từ interferon β sang phương pháp điều trị khác: - Dù điều trị nền là gì: Không cần trì hoãn nếu đáp ứng bilan trước điều trị bình thường. Chuyển sang Interferon β - Dù điều trị nền là gì: Không cần trì hoãn nếu đáp ứng bilan trước điều trị bình thường. | |
| Tiêm chủng vacin | - Tiêm chủng với lịch cộng đồng chung - Không có chống chỉ định với vắc-xin sống. | |
| TERIFLUNOMIDE | Chỉ định | - RRMS từ 10 tuổi |
| Liều | - 14 mg mỗi ngày một lần, uống. - Nếu cân nặng < 40 kg: 7 mg mỗi ngày một lần, uống. | |
| Chống chỉ định chính | - Suy gan nặng, suy thận nặng khi thận chu kỳ. - Giảm protein máu nặng (ví dụ: hội chứng thận hư). - Nhiễm trùng hoạt động nặng, chưa được kiểm soát. - Suy giảm miễn dịch nặng. | |
| Đánh giá trước điều trị cụ thể | - Huyết áp, CTM, AST, ALT βHCG - Huyết thanh VZV, HBV, HCV, HIV; QuantiFERON® | |
| Theo dõi cụ thể | - Trong trường hợp không có bất thường về gan và các liệu pháp điều trị độc gan khác (chống động kinh, chống trầm cảm), đánh giá chức năng gan mỗi tháng trong 6 tháng và sau đó cứ sau 2 tháng một lần. - AST, ALT ít nhất 4 tuần một lần trong 6 tháng và sau đó định kỳ hàng năm. - CTM phải được theo dõi thường xuyên (ít nhất là hàng năm). - Huyết áp nên được theo dõi thường xuyên trong quá trình điều trị. | |
| TERIFLUNOMIDE | Theo dõi cụ thể | Tăng đào thải thuốc - Cholestyramine 8g 3lần/ngày trong 11 ngày. - Sau đó, nếu đang có kế hoạch mang thai, 2 lần đo nồng độ thuốc trong huyết tương của teriflunomide (<0,02 mg/l) cách nhau 15 ngày. |
| Mang thai và cho con bú | - Ngừng Teriflunomide và thực hiện một quy trình loại bỏ nhanh chóng thuốc trước khi thụ thai. - Duy trì tránh thai của người phụ nữ khi nồng độ teriflunomide trong máu lớn hơn 0,02 mg/L. - Việc sử dụng teriflunomide chống chỉ định ở phụ nữ khi mang thai. - Không cho con bú ở những bệnh nhân được điều trị bằng teriflunomide. | |
| Chuyển đổi thuốc | Chuyển sang Teriflunomide: - Glatiramer acetate, Interferon β, Dimethyl fumarate, Fingolimod, Natalizumab: Không cần trì hoãn nếu bilan trước điều trị bình thường. - Ocrelizumab, Mitoxantrone: trì hoãn 3 tháng. - Alemtuzumab, Cladribine: Tùy thuộc vào đợt hoạt động trên lâm sàng hoặc MRI. Chuyển từ Teriflunomide sang điều trị khác Hướng tới điều trị bậc 1 hoặc bậc 2: Không trì hoãn nếu xét nghiệm trước điều trị bình thường và sau khi đã thải trừ thuốc | |
| Tiêm chủng vacin | - Lịch tiêm chủng cho dân số nói chung - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm hàng năm và phế cầu khuẩn, bạch hầu-ho gà-uốn ván 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Chống chỉ định Vắc-xin sống giảm độc lực (Thủy đậu, sởi, quai bị, rubella, sốt vàng). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin sởi, quai bị, rubella và sốt vàng, 6 tuần trước khi bắt đầu điều trị vắc-xin thủy đậu. | |
| DIMETHYLE FUMARATE và DIROXIMEL FUMARATE | Chỉ định | - RRMS từ 18 tuổi |
| Liều | - Dimethyle fumarate 120 mg (1 viên) X 2, uống chia 2 mỗi ngày vào giữa bữa ăn trong ít nhất 7 ngày, sau đó 240 mg (1 viên) X 2 /uống mỗi ngày vào giữa bữa ăn được tiếp tục. - Diroximel fumarate 231 mg (1viên) X 2, uống chia 2 mỗi ngày vào giữa bữa ăn trong ít nhất 7 ngày, sau đó 462 mg (2 viên) X 2, uống chia 2 mỗi ngày vào giữa bữa ăn được tiếp tục. | |
| Chống chỉ định chính | - Suy giảm miễn dịch liên quan đến giảm bạch cầu lympho -Nhiễm trùng cơ hội (PML). | |
| Đánh giá trước điều trị cụ thể | - CTM, AST, ALT, ure, creatinin, protein niệu - Huyết thanh học VZV, HBV, HCV, HIV; QuantiFERON® được cân nhắc theo cơ địa | |
| Theo dõi cụ thể | CTM, ASAT, ALAT, urê, creatinine cứ mỗi 3 tháng. | |
| Mang thai và cho con bú | - Điều trị bằng DMF có thể được tiếp tục cho đến khi có thai được chẩn đoán. - Nên ngừng DMF ngay sau khi chẩn đoán mang thai. - Cho con bú không được khuyến cáo ở những bệnh nhân được điều trị bằng DMF | |
| DIMETHYLE FUMARATE và DIROXIMEL FUMARATE | Chuyển đổi thuốc | Chuyển từ DMF sang điều trị khác: - Không cần trì hoãn nếu số lượng lympho ≥ 800/mm3. Chuyển sang DMF: - Glatiramer Acetate và Interferon β: Không cần trì hoãn - Fingolimod: Khi mức lympho được bình thường hóa (≥1000/mm3). - Teriflunomide: Sau quá trình thải trừ thuốc. - Natalizumab: Không cần trì hoãn điều trị nếu bilan trước điều trị bình thường. - Mitoxantrone: Trì hoãn 3 tháng hoặc đến khi lympho ≥1000/mm3. - Ocrelizumab: ≥ 3 tháng sau đợt điều trị cuối cùng nếu đánh giá trước điều trị đáp ứng được - Cladribine: Nếu có đợt tái hoạt động trên lâm sàng hoặc MRI và xét nghiệm trước điều trị bình thường |
| Tiêm chủng vacin | - Lịch tiêm chủng cho dân số nói chung - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm hàng năm và phế cầu, bạch hầu-ho gà - uốn ván mỗi 10 năm, thủy đậu và VGB nếu xét nghiệm âm tính, covid mỗi 6 tháng. - Chống chỉ định vắc-xin sống giảm độc lực: (Thủy đậu, sởi, quai bị, rubella, sốt vàng). Trong trường hợp cần thiết, cần có kế hoạch tiêm đầy đủ 4 tuần trước khi bắt đầu điều trị với sởi quai bị rubella và sốt vàng; 6 tuần trước khi bắt đầu điều trị với vaccin thủy đậu | |
| FINGOLIMOD | Chỉ định | - MS hoạt động mạnh dù đã trải qua ít nhất 1 điều trị hoàn chỉnh ở bệnh nhân từ 10 tuổi trở lên - RRMS nặng hoặc tiến triển nhanh: từ 2 đợt tái phát không gây tàn tật trong 1 năm hoặc ít nhất 1 tổn thương ngấm thuốc hoặc tăng kích thước có ý nghĩa trên T2 ở bệnh nhân từ 10 tuổi trở lên |
| Liều | - Người lớn và trẻ em > 40 kg: 1 viên 0,5mg/ngày - Trẻ em < 40 kg (≥ 10 tuổi): 1 viên 0,25 mg/ngày | |
| Chống chỉ định chính | - Suy giảm miễn dịch (ức chế miễn dịch hoặc liệu pháp khác). - Nhiễm trùng hoạt động nặng, nhiễm trùng hoạt động mãn tính (viêm gan, lao). - Ung thư tiến triển. - Suy gan nặng (Child-Pugh C). - Trong 6 tháng cuối nhồi máu cơ tim, đau thắt ngực không ổn định, đột quỵ/TIA, suy tim mất bù. - Điều trị nhịp tim chậm; BAV cấp II, Mobitz II hoặc BAV III; QTc ≥500 miligiây. | |
| Đánh giá trước điều trị cụ thể | - CTM, ASAT, ALT, bilirubin < 6 tháng +/- β-HCG. - Huyết thanh VZV, HBV, HCV, HIV; QuantiFERON® sẽ được cân nhắc theo cơ địa - Tầm soát ung thư cổ tử cung (phụ nữ HPV từ 25 đến 65 tuổi). - ECG. - Khám da liễu (nguy cơ ung thư biểu mô/khối u ác tính tế bào đáy). - Khám mắt nếu tiền sử bệnh tiểu đường hoặc viêm màng bồ đào (nguy cơ phù hoàng điểm). - MRI < 3 tháng (kiểm tra các dấu hiệu của PML). | |
| FINGOLIMOD | Theo dõi cụ thể | - Liều thứ 1: mạch và huyết áp mỗi giờ trong 6 giờ sau đó ECG ở giờ 6. - CTM ở tháng 3, sau đó thường xuyên ít nhất 1 lần /năm hoặc nếu có dấu hiệu nhiễm trùng → Ngừng Fingolimod nếu Lympho < 200/mm3. - AST, ALT, bilirubin ở tháng 1, 3, 6, 9, 12 tháng sau đó thường xuyên - Khám da liễu hàng năm. - Đáy mắt : 3-4 tháng sau khi bắt đầu điều trị. |
| Mang thai và cho con bú | - Mang thai: chống chỉ định với Fingolimod. - Ngừng Fingolimod 2 tháng trước khi ngừng tránh thai. - Bắt đầu nhanh chóng điều trị tương thích với thai kỳ để ngăn ngừa sự bùng cơn lại - Ngừng Fingolimod nếu mang thai + báo cáo cảnh giác dược. - Chống chỉ định cho con bú ở những bệnh nhân được điều trị bằng Fingolimod. | |
| Chuyển đổi thuốc | Chuyển sang Fingolimod: - Glatiramer Acetate và Interferon β: Không cần trì hoãn. - Dimethyl fumarate: Khi mức Lympho (≥1000 / mm3) ngoại trừ các trường hợp ngoại lệ được thảo luận trong hội chẩn đa chuyên khoa (≥ 800/mm3). - Teriflunomide: Sau quá trình thải trừ thuốc - Natalizumab: Trì hoãn 1 tháng sau liều cuối cùng nếu xét nghiệm JCV + MRI mỗi 3 tháng cho đến 6 tháng kết thúc điều trị natalizumab - Ocrelizumab: ít nhất 3 tháng kể từ liều cuối cùng nếu xét nghiệm trước điều trị bình thường; thời gian trì hoãn nên được thảo luận trong các staff về MS - Mitoxantrone: Khi lympho ≥ 1000/mm3 và thời gian trì hoãn được bàn luận trong các buổi hội chẩn về MS (3-6 tháng) - Cladribine: Nếu có đợt tái hoạt động trên lâm sáng hoặc MRI và xét nghiệm trước điều trị bình thường Chuyển từ Fingolimod sang phương pháp điều trị khác - Bắt đầu một đợt điều trị khác sau khi ngừng Fingolimod để giảm nguy cơ khi ngừng thuốc bệnh tiến triển bùng phát nặng hơn - Bậc 1: Không cần trì hoãn điều trị nếu bilan trước khi điều trị bình thường. - Natalizumab hoặc Ocrelizumab: 1 tháng và đánh giá trước điều trị cho phép liệu pháp bắc cầu (đánh giá trước điều trị không tính đến giảm bạch cầu từ nguy cơ dội lại). | |
| Tiêm chủng vacin | - Lịch tiêm chủng của dân số nói chung (kiểm tra HPV +++) - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm hàng năm và phế cầu khuẩn, bạch hầu-ho gà - uốn ván mỗi 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Chống chỉ định Vắc-xin sống giảm độc lực được (VZV, sốt vàng da, v.v.). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin, sốt vàng da, 6 tuần trước khi bắt đầu điều trị vắc-xin VZV. - Người chăm sóc: lịch tiêm chủng cho dân số nói chung + cúm + VZV nếu huyết thanh âm tính. | |
| PONESIMOD và OZANIMOD | Chỉ định | - Người lớn RRMS thể hoạt động, biểu hiện bằng lâm sàng và hình ảnh học (ưu tiên) |
| Liều | - PONVORY® + Liệu pháp khởi động 14 ngày: D1 uống 1 viên 2 mg/ngày sau đó tăng dần lên 10 mg/ngày + Liều duy trì từ D15: 1 viên 20 mg/ngày + Trong trường hợp quên/gián đoạn: *Nếu ít hơn 4 liều liên tiếp, lặp lại liều đã quên đầu tiên *Nếu 4 lần liên tiếp trở lên, lặp lại quy trình ban đầu - ZEPOSIA® + Liệu pháp khởi động 7 ngày D1 → D14: 0,23 mg trong 1 viên/ngày D5 → D7: 0,46 mg trong 1 viên/ngày + Liều duy trì từ D8: 0,92 mg trong 1 viên/ngày + Trong trường hợp quên/gián đoạn → Tương đương kế hoạch điều trị ban đầu nếu (bắt đầu lại từ đầu) nếu: Nếu ≥1 ngày giữa D1 và D14 Nếu ≥7 ngày liên tiếp giữa D15 và D28 Nếu ≥14 ngày liên tiếp sau D28 | |
| Chống chỉ định chính | Chống chỉ định với bệnh nhân có tiền sử nhồi máu cơ tim, cơn đau thắt ngực không ổn định, cơn thiếu máu não thoáng qua trong 6 tháng, suy tim mất bù hoặc suy tim độ III – IV theo NYHA, rối loạn nhịp tim. | |
| Đánh giá trước điều trị cụ thể | Công thức máu, chức năng gan thận, ECG, VZV IgG, chụp đáy mắt | |
| Theo dõi cụ thể | - Điều trị ngoại trú lần 1 - Liều thứ 1 trong viện với theo dõi trong 4 giờ đối với Ponesimod và 6 giờ đối với Ozanimod sau khi tư vấn tim mạch nếu: + Nhịp tim chậm xoang<55 nhịp/phút + BAV I hoặc BAV II loại Mobitz I + Tiền sử NMCT hoặc suy tim trong vòng 6 tháng trước + Đáy mắt: không có hệ thống nhưng được thực hiện trong trường hợp khiếu nại trực quan + Ozanimod: Theo dõi huyết áp thường xuyên | |
| Mang thai và cho con bú-chuyển đổi thuốc | - Ngừng Ponesimod 1 tuần trước khi ngừng tránh thai. - Ngừng Ozanimod 3 tháng trước khi ngừng tránh thai. | |
| Tiêm chủng vắc-xin | - Ozanimod: Trì hoãn khởi đầu điều trị sau 4 tuần tiêm chủng; tránh tiêm vắc-xin sống và giảm độc lực trong vòng 3 tháng điều trị. - Ponesimod: Trì hoãn khởi đầu điều trị sau 4 tuần tiêm chủng; tránh tiêm vắc-xin sống và giảm độc lực trong vòng 1 - 2 tuần sau điều trị. | |
| NATALIZUMAB | Chỉ định | - RRMS rất hoạt động mặc dù liệu pháp thay đổi bệnh được tiến hành tốt từ năm 18 tuổi - Ngay từ đầu cho MS tái phát nếu ít nhất 2 lần tái phát nặng trong năm liên quan đến 1 hoặc nhiều tổn thương tăng tín hiệu đối quang từ hoặc tăng số lượng tổn thương T2 mới từ 18 tuổi |
| Liều | - Truyền TM (300 mg trong 1 giờ) hoặc tiêm dưới da (2 lần 150 mg ở 2 vùng) mỗi 4 tuần ở trong bệnh viện - Sau đó tiêm và 1 giờ theo dõi trong 6 tháng đầu | |
| Chống chỉ định chính | - Tiền sử dùng ức chế miễn dịch hoặc nhiễm trùng cơ hội. - Ung thư tiến triển. - Quá mẫn cảm với Natalizumab hoặc bất kỳ tá dược nào. | |
| Đánh giá trước điều trị cụ thể | - Xét nghiệm huyết thanh vi-rút JC - MRI não trong vòng dưới 3 tháng - Huyết thanh HBV, HCV, VZV, HIV, QuantiFERON® sẽ được thảo luận theo cơ địa - CTM, đếm tế bào lympho B và T, CD4 / CD8, định lượng IgG - AST, ALT | |
| Theo dõi cụ thể | Theo dõi cụ thể - Trong trường hợp huyết thanh JC âm tính. + Xét nghiệm huyết thanh JC 6 tháng một lần. + MRI não hàng năm. - Nếu huyết thanh JC dương tính và theo chỉ số, thảo luận về việc tiếp tục Natalizumab và các phương thức theo dõi (Tần suất chụp MRI và huyết thanh JC). - Xét nghiệm kháng thể kháng Natalizumab trong trường hợp có phản ứng liên quan đến truyền dịch hoặc điều trị không hiệu quả. | |
| Mang thai và cho con bú | + Điều trị bằng Natalizumab có thể được tiếp tục cho đến khi mang thai được chẩn đoán. + Nên thảo luận về việc có nên tiếp tục điều trị trong khi mang thai trong một cuộc họp tư vấn hay không. +Khoảng cách liều có thể được thảo luận trong khi mang thai. +Điều trị bằng Natalizumab có thể được tiếp tục trong hai quý đầu của thai kỳ. +Tiếp tục hoặc nối lại Natalizumab trong quý ba của thai kỳ có thể được thảo luận theo mức độ nghiêm trọng của bệnh lý. + Nếu ngừng điều trị, nên nối lại Natalizumab càng sớm càng tốt sau khi sinh. + Có thể cân nhắc cho con bú ở những bệnh nhân được điều trị bằng Natalizumab. | |
| Chuyển đổi thuốc | Chuyển sang Natalizumab + Glatiramer Acetate và Interferon β: Không cần trì hoãn điều trị nếu xét nghiệm tiền trị liệu bình thường. + Dimethyl fumarate: khi mức Lympho chuẩn hóa (≥1000 /mm3), ngoại trừ các trường hợp ngoại lệ được thảo luận trong RCP/CRC-SEP (≥ 800 / mm3). + Teriflunomide: Sau khi tăng thải trừ thuốc. + Fingolimod: Nếu xét nghiệm trước điều trị bình thường hoặc trì hoãn 1 tháng | |
| NATALIZUMAB | Chuyển đổi thuốc | + Ocrelizumab: Hoãn 3 tháng. + Alemtuzumab, Cladribine: Dựa trên phục hồi lâm sàng hoặc MRI. Chuyển từ Natalizumab sang phương pháp điều trị khác + Hướng tới điều trị bậc 1: Không cần trì hoãn. + Hướng tới điều trị bậc 2: Trì hoãn 1 tháng. Thận trọng - Thông tin + Khi ngừng điều trị: nguy cơ dội lại và gây hoạt động bệnh - Điều trị bắc cầu sớm bằng một phương pháp điều trị thay đổi bệnh khác. - MRI và theo dõi lâm sàng sau 3 và 6 tháng sau lần tiêm cuối cùng (nguy cơ PML sau ngừng) nếu huyết thanh JC dương tính. |
| Tiêm chủng vacin | Tiêm phòng: các bước trước khi bắt đầu Natalizumab - Lịch tiêm chủng cho dân số nói chung - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là hàng năm cúm và phế cầu khuẩn, DTP 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Vắc-xin sống giảm độc lực được chống chỉ định (VZV, sốt vàng da, v.v.). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin, sốt vàng da, 6 tuần trước khi bắt đầu điều trị vắc-xin VZV. | |
| KHÁNG THỂ KHÁNG CD20 | Chỉ định | - Ocrelizumab: MS thể hoạt động, bất kể dạng nào từ 18 tuổi - Ofatumumab: RRMS hoặc MS hoạt động từ 18 tuổi - Rituximab: Chỉ định nhãn phụ (không nằm trong các chỉ định điều trị chính trong quá trình xét duyệt lưu hành trên thị trường) |
| Liều | - Ocrelizumab 300 mg IV D1, D15 sau đó 600 mg IV mỗi 6 tháng. - Ofatumumab 20 mg tiêm DD ở D0, D7, D14, D28 và mỗi 4 tuần. - Rituximab: 1g IV D1 và D15 sau đó 1g IV mỗi 6 tháng. | |
| Chống chỉ định chính | - Nhiễm trùng hoạt động/viêm gan B hoạt động. - Suy giảm miễn dịch nặng. - Bệnh lý ác tính hoạt động. - Thận trọng trên BN suy tim. | |
| Đánh giá trước điều trị cụ thể | - CTM, ASAT, ALT - Huyết thanh học HBV, HCV, HIV, VZV - Xét nghiệm định lượng Ig, QuantiFERON® sẽ được thảo luận theo cơ địa - Kiểm tra điện tim, siêu âm tim (Chú ý người lớn tuổi, có bệnh lý tim mạch kèm theo) | |
| Theo dõi cụ thể | - CTM, đo lượng Ig 6 tháng một lần - Trong trường hợp giảm IgG, thảo luận về chỉ định bổ sung IV IgG. Nếu viêm gan B được biết đã khỏi, hội chẩn bác sĩ tiêu hóa để theo dõi cụ thể chặt chẽ hoặc điều trị kháng vi rút liên quan | |
| KHÁNG THỂ KHÁNG CD20 | Mang thai và cho con bú | - Cần trị hoãn ít nhất 2 tháng giữa lần tiêm kháng CD20 cuối cùng (ocrelizumab hoặc Rituximab) và ngừng tránh thai. Thời gian này là 6 tháng đối với Ofatumumab. + Khoảng cách truyền dịch có thể được xem xét để kéo dài thời gian thụ thai. + Có thể cân nhắc cho con bú với Anti-CD20 ngoại trừ Ofatumumab. |
| Chuyển đổi thuốc | Chuyển sang Anti-CD20 + Glatiramer Acetate và Interferon β: Không cần trì hoãn điều trị nếu bilan trước điều trị bình thường. + Fingolimod: Trì hoãn 1 tháng và/hoặc xét nghiệm trước điều trị bình thường. + Teriflunomide: Sau quy trình loại bỏ nhanh chóng và bilan trước điều trị bình thường. + Dimethyl fumarate: Lympho ≥ 800/mm3 +NatalizumabTrì hoãn 1 tháng và đánh giá trước điều trị bình thường. + Mitoxantrone: Trì hoãn từ 3 đến 6 tháng hoặc khi mức Lympho ≥ 1000 / mm3 (sẽ được thảo luận trong hội chẩn đa chuyên khoa). + Cladribine: Có hoạt động lâm sàng hoặc MRI và nếu bilan trước điều trị bình thường. Chuyển từ Anti-CD20 sang phương pháp điều trị khác + Trì hoãn 3 tháng và đánh giá tiền điều trị bình thường. + Thảo luận về khung thời gian ngắn hơn trong hội chẩn đa chuyên khoa nếu cần thiết. | |
| Tiêm chủng vacin | Các biện pháp trước khi bắt đầu Anti-CD20 - Lịch tiêm chủng của dân số nói chung (kiểm tra HPV +++) - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm hàng năm và phế cầu khuẩn DTP 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Vắc-xin sống giảm độc lực được chống chỉ định (VZV, sốt vàng da, v.v.). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin, sốt vàng da, 6 tuần trước khi bắt đầu điều trị vắc-xin VZV. - Người chăm sóc: lịch tiêm chủng cho dân số nói chung + cúm + VZV nếu huyết thanh âm tính. | |
| CLADRIBINE | Chỉ định | - RRMS từ 18 tuổi trở lên và hoạt động được xác định bởi các thông số lâm sàng hoặc MRI: - Theo (các) phương pháp điều trị thay đổi bệnh khác: 1 lần tái phát trong năm trước và ≥ 1 tổn thương ngấm thuốc đối quang từ trên T1 hoặc ≥ 9 tổn thương T2 - Hoặc ≥ 2 đợt bùng phát trong năm trước Xác nhận bởi hội chẩn đa chuyên khoa |
| Liều | - 2 chu kỳ cách nhau 1 năm. - Liều dùng dựa trên trọng lượng: 1,75 mg / kg/năm, trong 2 năm = 3,5 mg/kg. - Mỗi chu kỳ = 1 đến 2 viên/ngày trong 4 đến 5 ngày sau đó lặp lại 28 ngày + sau đó. - Không điều trị bắc cầu trong trường hợp không có hoạt động viêm. | |
| Chống chỉ định chính | - BN suy giảm miễn dịch / Lympho <1000/mm3. - Bệnh ác tính tiến triển. - Nhiễm trùng hoạt động mãn tính (lao phổi hoặc viêm gan) / HIV /PML. - Suy thận vừa hoặc nặng (độ thanh thải creatinin <60 ml/phút). - Tiền sử rối loạn chức năng gan / Độc tính với gan do thuốc. | |
| CLADRIBINE | Đánh giá trước điều trị cụ thể | - Cần được kiểm tra trước mỗi chu kỳ - CTM, urê, creatinine, AST, ALT, phosphatase kiềm, bilirubin toàn phần. - Tế bào lympho trước chu kỳ 1 < 1000/mm3 →Cladribine chống chỉ định - Tế bào lympho trước chu kỳ 2 ≤ 800/mm3 → dịch chuyển chu kỳ 2 - Độ thanh thải creatinine≥ 60 ml/phút -Huyết thanh HBV, HCV, VZV, HIV, QuantiFERON® - βHCG. |
| Theo dõi cụ thể | - Cần được kiểm tra trước mỗi chu kỳ - CTM, urê, creatinine, AST, ALT, phosphatase kiềm, bilirubin toàn phần Tế bào lympho trước chu kỳ 1 < 1000/mm3 →Cladribine chống chỉ định -Tế bào lympho trước chu kỳ 2 ≤ 800/mm3 → dịch chuyển chu kỳ 2 - Độ thanh thải creatinine≥ 60 ml/phút - Huyết thanh HBV, HCV, VZV, HIV, QuantiFERON® - βHCG. Theo dõi cụ thể CTM, ASAT, ALT, phosphatase kiềm, bilirubin toàn phần: 2 tháng và 6 tháng sau khi bắt đầu mỗi chu kỳ. + Tế bào lympho≤ 500/mm3→ Theo dõi sinh học + lâm sàng chặt chẽ hơn (Herpes zoster) + Tế bào lympho≤ 200/mm3→ valaciclovir 500 mg/ngày lên đến Lympho > 200/mm3 + Nếu chức năng gan bất thường, đối chiếu theo dõi sinh học và lâm sàng. | |
| Mang thai và cho con bú | - Mang thai sớm và cho con bú chống chỉ định với Cladribine. - Cho dù bệnh nhân là phụ nữ hay nam giới, không thụ thai trong quá trình điều trị và tối đa 6 tháng sau lần uống cuối cùng. | |
| Chuyển đổi thuốc | Chuyển sang Cladribine: - Chỉ định được xác nhận bởi hội chẩn liên khoa - Glatiramer Acetate và Interferon β: Không cần trì hoãn - Fingolimod và Dimethyl fumarate: Công thức máu mỗi 1 đến 2 tuần sau khi ngưng cho đến khi đạt được mức Lympho ≥ 1000 / mm3. - Teriflunomide: Sau khi tăng thải trừ thuốc. - Natalizumab, Ocrelizumab, Mitoxantrone: Thời gian trì hoãn phải được thảo luận trong hội chẩn liên khoa Chuyển Cladribine sang phương pháp điều trị khác - Điều trị mới (bậc 1 và bậc 2) khi hoạt động lâm sàng hoặc MRI xuất hiện trở lại (MRI hàng năm) và nếu đánh giá tiền điều trị ổn định. | |
| Tiêm chủng vacin | - Lịch tiêm chủng cho dân số nói chung - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm hàng năm và phế cầu khuẩn DTP 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Vắc-xin sống giảm độc lực được chống chỉ định (VZV, sốt vàng da...). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin, sốt vàng da, 6 tuần trước khi bắt đầu điều trị vắc-xin VZV. - Người chăm sóc: lịch tiêm chủng cho dân số nói chung + cúm + VZV nếu huyết thanh âm tính. | |
| MITOXANTRONE | Chỉ định | Các dạng MS hoạt động - ≥ 2 lần tái phát di chứng trong năm và ≥ 1 tổn thương hoạt động trên MRI. - Hoặc tình trạng khuyết tật tiến triển nhanh và ≥ 1 tổn thương hoạt động trên MRI. |
| Liều | 3-6 đợt hàng tháng ở mức 12 mg/m2; Liều tích lũy tối đa 72 mg/m2. | |
| Chống chỉ định chính | - Bệnh nhân suy giảm miễn dịch / Lympho <900/mm3. - Bệnh ác tính/bệnh máu tiến triển. - Nhiễm trùng hoạt động cấp tính hoặc mãn tính. - Suy gan nặng. - Bệnh tim/ EF < 50%. | |
| Đánh giá trước điều trị cụ thể | Đánh giá tiền điều trị cụ thể - CTM, điện giải, urê, creatinine, ASAT, ALT, CRP. - Huyết thanh VZV, HBV, HCV, HIV. - ECG và siêu âm tim (EF > 50%). - Nếu gợi ý nhiễm trùng lâm sàng → đánh giá định hướng (tình trạng răng miệng, ho, v.v.). - Trữ đông trứng nếu cần | |
| Theo dõi cụ thể | Theo dõi cụ thể - ECG, TPT nước tiểu, βHCG trước mỗi đợt điều trị - CTM 10 ngày sau mỗi đợt điều trị và trong vòng 5 ngày trước lần điều trị tiếp theo →CTM bình thường trên D5 và giảm bạch cầu trung tính trên D10 BCTT ≥ 500 → Mitoxantrone 20mg BCTT < 500 → Mitoxantrone 10 mg →CTM bất thường trên D-5 Giảm bạch cầu< 2000/mm3 → hoãn điều trị Giảm bạch cầu trung tính < 1500/mm3 → hoãn điều trị - Siêu âm tim tại tháng 6 sau đó hàng năm trong 5 năm. CTM cứ sau 3 tháng trong 5 năm | |
| Mang thai và cho con bú | - Mitoxantrone chống chỉ định với phụ nữ thai kì sớm và cho con bú. - Sử dụng các biện pháp tránh thai (cả nam và nữ) trong quá trình điều trị và kéo dài ít nhất 6 tháng sau khi kết thúc đợt điều trị. | |
| Chuyển đổi thuốc | Chuyển sang Mitoxantrone: - Glatiramer Acetate và Interferon β: Không cần trì hoãn - Teriflunomide: Sau khi tăng tốc thủ tục xử lý. - Fingolimod và Dimethyl fumarate, Natalizumab, Ocrelizumab: Khung thời gian/tỷ lệ Lympho sẽ được thảo luận đa chuyên khoa. - Cladribine: Nếu có lâm sàng hoặc MRI và nếu đánh giá trước điều trị ổn. Chuyển từ Mitoxantrone sang điều trị khác - Bậc 1 : Trì hoãn từ 0 đến 3 tháng sau đợt điều trị cuối cùng nếu đánh giá tiền điều trị ổn. - Bậc 2 : Trì hoãn từ 3 đến 6 tháng sau đợt điều trị cuối cùng sẽ được thảo luận trong đa chuyên khoa. | |
| MITOXANTRONE | Tiêm chủng vacin | Tiêm chủng: Các bước trước khi bắt đầu Mitoxantrone - Lịch tiêm chủng cho dân số nói chung - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm và phế cầu khuẩn hàng năm, DTP 10 năm/lần, VZV và HBV nếu huyết thanh âm tính, Covid 6 tháng/lần). - Vắc-xin sống giảm độc lực được chống chỉ định (VZV, sốt vàng da, v.v.). Nếu cần thiết, hoàn thành lịch tiêm chủng 4 tuần trước khi bắt đầu điều trị vắc-xin, sốt vàng da, 6 tuần trước khi bắt đầu điều trị vắc-xin VZV. - Người chăm sóc: lịch tiêm chủng cho dân số nói chung + cúm + VZV nếu huyết thanh âm tính. |
| AZATHIOPRINE (Dành cho trường hợp không có các thuốc điều trị khác, chất lượng bằng chứng hiệu quả không cao) | Chỉ định | MS thể tái phát |
| Liều | - Liều khởi đầu là 1mg/kg/ngày, chia làm một hoặc hai lần trong ngày. - Liều lượng tăng dần mỗi 4-6 tuần để đạt liều duy trì 2,5 – 3 mg/kg/ngày (tổng liều 100-150mg/ngày). | |
| Chống chỉ định chính | Quá mẫn với Azathioprin Đang điều trị với nhóm alkyl hóa, gây tăng nguy cơ ung thư | |
| Đánh giá trước điều trị cụ thể | Không | |
| Theo dõi cụ thể | Cần theo dõi men AST, ALT và CTM sau tuần đầu tiên sử dụng sau đó thửu lại ở tháng thứ nhất sau khi tăng liều. Theo dõi số lượng bạch cầu và AST, ALT mỗi 2-3 tháng Cân nhắc ngừng thuốc hoặc hội chẩn đa chuyên khoa nếu số lượng bạch cầu hạt và hoặc tăng AST, ALT quá 3 lần giá trị giới hạn trên | |
| Mang thai và cho con bú - Chuyển đổi thuốc | Cho con bú: Azathioprin có bài tiết qua sữa mẹ, nên đình chỉ nuôi con bằng sữa mẹ. Nếu tiếp tục cho con bú, xét nghiệm máu toàn phần, chức năng gan ở trẻ, không cho con bú trong vòng 4-6 giờ sau khi uống thuốc. | |
| Tiêm chủng vacxin | - Lịch tiêm chủng cho dân số nói chung. - Không có chống chỉ định với vắc-xin sống. | |
| MYCOPHENOLATE MOFETIL (Dành cho trường hợp không có các thuốc điều trị khác, chất lượng bằng chứng hiệu quả không cao) | Chỉ định | Đơn trị liệu hoặc phối hợp với các thuốc điều hòa miễn dịch khác trong RRMS |
| Liều | Khởi đầu 500mg/ngày trong tuần đầu, sau đó tăng lên 500mg/ngày mỗi tuần đến khi đạt liều 2000mg/ngày, tiếp tục trong 12 tháng. | |
| Chống chỉ định chính | Quá mẫn với Mycophenalate mofetil hoặc bất kỳ thành phần nào của thuốc Bệnh nhân dị ứng với Polysorbate 80 | |
| Đánh giá trước điều trị cụ thể | CTM, ALT, AST, urê, creatinine. | |
| Theo dõi cụ thể | Công thức máu, chức năng gan thận mỗi tuần trong 1 tháng đầu, mỗi 2 tuần trong 2 tháng tiếp theo, sau đó là mỗi tháng. | |
| HƯỚNG DẪN SỬ DỤNG THUỐC | ||
| MYCOPHENOLATE MOFETIL (Dành cho trường hợp không có các thuốc điều trị khác, chất lượng bằng chứng hiệu quả không cao) | Mang thai và cho con bú | Mang thai và cho con bú: Mycophenolate mofetil chống chỉ định với các thai phụ sớm và cho con bú, cả nam và nữ cần có biện pháp tránh thai trước và kéo dài sau điều trị 6 tháng |
| Tiêm chủng vacxin | - Lịch tiêm chủng cho dân số nói chung. - Không có chống chỉ định với vắc-xin sống. - Lịch tiêm chủng cho bệnh nhân suy giảm miễn dịch (đặc biệt là cúm và phế cầu khuẩn hàng năm, DTP 10 năm/lần, VZV và HBV nếu huyết thanh âm tính) | |
5.5. Điều trị bệnh MS ở bệnh nhân có thai và cho con bú MS là phổ biến nhất ở phụ nữ trong độ tuổi sinh đẻ và điều này đặt ra nhiều thách thức hơn cho phụ nữ, gia đình của họ và cung cấp các dịch vụ y tế. Khái niệm MS dường như không có ảnh hưởng đến sinh lý sinh sản mặc dù rối loạn chức năng tình dục ảnh hưởng đến người mắc MS, có thể ảnh hưởng đến thụ thai. Quản lý việc mang thai MS không thường xuất hiện hoặc tái phát trong thời kỳ mang thai. Nhiều nghiên cứu chỉ ra tỷ lệ tái phát giảm khi mang thai nhưng tăng lên trong 3 tháng đầu sau khi sinh. Chăm sóc trước sinh ở BN MS tương tự như BN không MS nhưng một số có thể có rối loạn chức năng tiết niệu và ruột trầm trọng hơn, họ có thể dễ bị nhiễm trùng đường tiết niệu và viêm bể thận nếu không được điều trị. Điều trị thuốc Thiếu dữ liệu về độ an toàn của steroid ở BN MS có thai. Một vài nghiên cứu chỉ ra steroid làm tăng nguy cơ hở môi và hở hàm ếch khi sử dụng trong 3 tháng đầu của thai kỳ. Do đó cần cân nhắc cẩn thận giữa rủi ro/ lợi ích trước khi dùng steroid cho các trường hợp tái phát cấp tính xảy ra trong thai kỳ, đặc biệt trong 3 tháng đầu.20,30 Các lựa chọn thay thế như IVIG cũng có thể được xem xét.30 Hiện tại chưa thấy có bằng chứng nào cho thấy điều trị theo cơ chế bệnh sinh không gây quái thai hoặc an toàn trong thai kỳ. Nguy cơ gây quái thai và sảy thai thường được cân bằng với một cuộc thảo luận mở về khoảng thời gian ngừng DMT và khi nào nên bất đầu có thai. Đối với Interferon β, Glatiramer acetate, DMF một tháng đủ để ngừng điều trị trước khi thụ thai và 2 tháng đối với fingolimod. Mặc dù 3 tháng được khuyến cáo cho natalizumab nhưng có thể là 1 tháng.20,30 Các trị liệu điều trị triệu chứng nên được đánh giá đến các rủi ro tiềm ẩn gây quái thai do đó giảm thiểu những BN MS mang thai. Chỉ những trường hợp hoàn toàn cần thiết mới được sử dụng với liều hiệu quả tối thiểu. Chiến lược không dung thuốc được khuyến cáo. Hậu quả của việc mang thai Những nghiên cứu chỉ ra tỷ lệ phá thai, sinh mổ, sinh non và trẻ sơ sinh nhẹ cân tương đối cao ở những phụ nữ bị MS. Do đó những BN MS được khuyên là MS không tác động tiêu cực đến thai kỳ và hậu quả của nó. Các yếu tố sau sinh Vấn đề sinh nở: MS không ảnh hưởng đến vấn đề sinh nở và lựa chọn gây mê trong thai kỳ. Nuôi con bằng sữa mẹ: DMT không được khuyến khích trong thời kỳ cho con bú. DMT có thể được khởi động bắt đầu ngay sau sinh miễn là BN không cho con bú. Tránh thai: không thấy có bằng chứng nào cho thấy oestrogen có trong thuốc tránh thai có tác dụng phụ trên MS. Một số thuốc điều trị triệu chứng như carbamazepine có thể làm giảm tác dụng của thuốc tránh thai đường uống. BN MS bị giảm khả năng vận động nên được cảnh báo về nguy cơ huyết khối với thuốc tránh thai. Do đó các phương pháp ngừa thai thay thế nên được áp dụng. 5.6. Ghép tế bào gốc (hematopoietic stem cell transplantation) Ghép tế bào gốc là hướng điều trị cho những bệnh nhân xơ cứng rải rác tiến triển nặng dần, thường thất bại với những điều trị làm thay đổi quá trình bệnh sinh.33,34 Ghép tế bào gốc tự thân là hình thức ghép trong đó khối tế bào gốc của người bệnh được thu gom và lưu trữ, sau đó truyền trả lại cho người bệnh khi đã kết thúc điều kiện hóa nhằm phục hồi mô tạo máu. Tuy nhiên, đây là một kỹ thuật phức tạp, cần thực hiện theo quy trình nghiêm ngặt và đảm bảo các yêu cầu chuyên môn chặt chẽ.
6. PHÒNG BỆNH Tiêm vaccin phòng ngừa cúm, phế cầu, viêm gan B, thủy đậu. Khuyến khích người bệnh MS tập thể dục. Khuyên họ tập thể dục thường xuyên có thể có tác dụng có lợi trong bệnh MS và không có bất kỳ tác động có hại nào. Hút thuốc lá: Những người bị MS không nên hút thuốc lá.
TÀI LIỆU THAM KHẢO 1. Cree BAC, Hauser SL. Multiple Sclerosis,. Harrison’s Principles of Internal Medicine, . 20 ed. McGraw-Hill Education: New York, NY.; 2018. 2. MS International Federation. Atlas of MS 3rd edition. Part 1: Mapping multiple sclerosis around the world epidemiology findings. https://www.msif.org/wp-content/uploads/2020/10/Atlas-3rd-Edition-Epidemiology-report-EN-updated-30-9-20.pdf. 2020. 3. Mahad DH, Trapp BD, Lassmann H. Pathological mechanisms in progressive multiple sclerosis. Lancet Neurol 2015; 14(2): 183-93. 4. Wiendl H, Gold R, Berger T, et al. Multiple Sclerosis Therapy Consensus Group (MSTCG): position statement on disease-modifying therapies for multiple sclerosis (white paper). Ther Adv Neurol Disord 2021; 14: 17562864211039648. 5. Lublin FD. New multiple sclerosis phenotypic classification. Eur Neurol 2014; 72 Suppl 1: 1-5. 6. Kurtzke JF. Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS). Neurology 1983; 33(11): 1444-52. 7. The National Institute for Health and Care Excellence. Multiple sclerosis in adults: management. NICE guideline. https://www.nice.org.uk/terms-andconditions#notice-of-rights) 2022 8. Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018; 17(2): 162-73. 9. Baskaran AB, Grebenciucova E, Shoemaker T, Graham EL. Current Updates on the Diagnosis and Management of Multiple Sclerosis for the General Neurologist. J Clin Neurol 2023; 19(3): 217-29. 10. Toosy A, Ciccarelli O, Thompson A. Symptomatic treatment and management of multiple sclerosis. Handb Clin Neurol 2014; 122: 513-62. 11. Lim EC, Seet RC. Use of botulinum toxin in the neurology clinic. Nat Rev Neurol 2010; 6(11): 624-36. 12. World health Organization. Proposal for inclusion of multiple sclerosis disease-modifying therapies (DMTs) on the complementary WHO Model Lists of Essential Medicines. World health Organization. 2022. 13. Yamout B, Sahraian M, Bohlega S, et al. Consensus recommendations for the diagnosis and treatment of multiple sclerosis: 2019 revisions to the MENACTRIMS guidelines. Mult Scler Relat Disord 2020; 37: 101459. 14. Wise J. Multiple sclerosis: NICE recommends treatment for secondary progressive MS. BMJ 2020; 371: m3990. 15. Hauser SL, Cree BAC. Treatment of Multiple Sclerosis: A Review. Am J Med 2020; 133(12): 1380-90 e2. 16. Zéphir H, Durand-Dubief F, Le -Page E. Fiches pratiques thérapeutiques pour la prise en charge des patients atteints de sclérose en plaques. Practical treatment sheets for multiple sclerosis. Pratique Neurologique 2023; 14(2):: 98-107. 17. Limmroth V. Treatment of relapsing-remitting multiple sclerosis: current and future algorithms. Eur Neurol 2014; 72 Suppl 1: 35-8. 18. Carod-Artal FJ, Adjamian P, Vila Silvan C, Bagul M, Gasperini C. A systematic review of European regional and national guidelines: a focus on the recommended use of nabiximols in the management of spasticity in multiple sclerosis. Expert Rev Neurother 2022; 22(6): 499-511. 19. Giovannoni G, Soelberg Sorensen P, Cook S, et al. Safety and efficacy of cladribine tablets in patients with relapsing-remitting multiple sclerosis: Results from the randomized extension trial of the CLARITY study. Mult Scler 2018; 24(12): 1594-604. 20. Lee M, O’Brien P. Pregnancy and multiple sclerosis. J Neurol Neurosurg Psychiatry 2008; 79(12): 1308-11. 21. Reeve K, On BI, Havla J, et al. Prognostic models for predicting clinical disease progression, worsening and activity in people with multiple sclerosis. Cochrane Database Syst Rev 2023; 9(9): CD013606. 22. Rae-Grant A, Day GS, Marrie RA, et al. Practice guideline recommendations summary: Disease-modifying therapies for adults with multiple sclerosis: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology. Neurology 2018; 90(17): 777-88. 23. The National Institute for Health and Care Excellence. Cladribine for treating relapsing–remitting multiple sclerosis. NICE guideline. https://www.nice.org.uk/guidance/ta616). 2019. 24. Dargahi N, Katsara M, Tselios T, et al. Multiple Sclerosis: Immunopathology and Treatment Update. Brain Sci 2017; 7(7). 25. Ministry of Health Malaysia. Management of multiple sclerosis. Clinical practice guidelines MOH/P/PAK/293.15(GU). 2015. 26. Montalban X, Gold R, Thompson AJ, et al. ECTRIMS/EAN guideline on the pharmacological treatment of people with multiple sclerosis. Eur J Neurol 2018; 25(2): 215-37. 27. Thompson AJ. Commentary on the ECTRIMS-EAN guideline for pharmacological treatment of multiple sclerosis. Ther Adv Neurol Disord 2018; 11: 1756286418770378. 28. Nonino F, Baldin E, Ridley B, Casetta I, Iuliano G, G. F. Azathioprine for people with multiple sclerosis (Protocol). Cochrane Database of Systematic Reviews 2021, Issue 7. Art. No.: CD015005. DOI: 10.1002/14651858.CD015005. 29. Ramo-Tello C, Blanco Y, Brieva L, et al. Recommendations for the Diagnosis and Treatment of Multiple Sclerosis Relapses. J Pers Med 2021; 12(1). 30. Coyle PK. Multiple sclerosis in pregnancy. Continuum (Minneap Minn) 2014; 20(1 Neurology of Pregnancy): 42-59. 31. Multiple Sclerosis International Federation. MSIF’s Off-Label Treatments recommendations for low-resource settings. https://www.msif.org/molt-guidelines-azathioprine-rituximab/. 2023. 32. Multiple Sclerosis International Federation. MSIF Essential Medicines Panel (MEMP) Guidelines for essential disease-modifying therapies for multiple sclerosis for low-resource settings. https://www.msif.org/wp-content/uploads/2023/01/MEMP_EtD-and-recommendations_public_201222.pdf. 2023. 33. Farge D, Labopin M, Tyndall A, et al. Autologous hematopoietic stem cell transplantation for autoimmune diseases: an observational study on 12 years’ experience from the European Group for Blood and Marrow Transplantation Working Party on Autoimmune Diseases. Haematologica 2010; 95(2): 284-92. 34. Miller AE, Chitnis T, Cohen BA, et al. Autologous Hematopoietic Stem Cell Transplant in Multiple Sclerosis: Recommendations of the National Multiple Sclerosis Society. JAMA Neurol 2021; 78(2): 241-6.