Nhân một trường hợp hội chứng Lewis-Sumner bị chẩn đoán nhầm TBMMN: lâm sàng, điểm lại y văn và các thách thức điều trị trên bệnh nhân VGSV B mạn tính.
NHÂN MỘT TRƯỜNG HỢP HỘI CHỨNG LEWIS-SUMNER BỊ CHẨN ĐOÁN NHẦM TBMMN: LÂM SÀNG, ĐIỂM LẠI Y VĂN CÁC THÁCH THỨC ĐIỀU TRỊ TRÊN BỆNH NHÂN VGSV B MẠN TÍNH
Ths.Bs. Lê Tự Quốc Tuấn
Bệnh viên đa khoa Triều An
- Ca lâm sàng
Tên bệnh nhân: Nguyễn Thị M. sinh năm 1963
Nghề nghiệp: thợ may
2. Bệnh sử:
Bệnh khởi phát vào khoảng tháng 5/2014 bệnh nhân bắt đầu có cảm giác tê bì và dị cảm như kiến bò ở các ngón chân (P), khoảng 1 tháng sau dị cảm lan ra bàn chân (P).Và 1 tháng tiếp sau đó dị cảm lan lên tới gối (P) và bệnh nhân bắt đầu có dị cảm ngón tay 1 và 2 (P) đồng thời có cảm giác yếu chân (P). Tình trạng bệnh diễn tiến nặng dần và đến ngày 28/7/2014 bệnh nhân phát hiện thấy yếu hẳn 1/2 người (P) nên đã đến khám và điều trị ngoại trú tại 1 bệnh viện nổi tiếng về chuyên ngành thần kinh tại Tp.Hồ Chí Minh với chẩn đoán nhồi máu não. Lúc này bệnh nhân điều trị đồng thời tại y học cổ truyền bệnh viện quận Tân Bình. Tình trạng bệnh không cải thiện và do công việc nên bệnh nhân quyết định điều trị tại phòng mạch ngoài giờ của 1 bác sĩ chuyên khoa đột quỵ đang công tác ở 1 bệnh viện công và tập vật lý trị liệu tại YHCT quận Tân Bình.
Sau 2 tháng bệnh không cải thiện và có dấu hiệu nặng dần: bệnh nhân xuất hiện thêm dị cảm bàn chân (T) và 2 ngón tay trỏ và cái (T), di chuyển phải có trợ giúp nên ngày 29/9 bệnh nhân đến khám tại bệnh viện Vạn Hạnh được chỉ định chụp MRI cột sống cổ và thắt lưng . Bệnh nhân được giới thiệu khám bs chuyên khoa Ngoại thần kinh và được chỉ định làm EMG và chụp MRI não. Kết quả MRI não bình thường và kết quả đo EMG phát hiện bệnh MADSAM(30/9/2014). Bệnh nhân đã điều trị đồng thời 2 bác sĩ chuyên khoa Nội thần kinh với: Methycobal và Nucleofort( Bs 1 ) , Lyrica và Encorate (bs 2). Bệnh tiếp tục diễn tiến nặng dần và vì bệnh nhân bị nhiễm VGSV B nên được đề nghị nhập viện điều trị với ImmunoGlobulin nhưng người nhà không có điều kiện. Đến ngày 17/10 bệnh nhân được giới thiệu tới tôi khám bệnh. Qua thăm khám lâm sàng , đo EMG lần 2 và nguyện vọng tha thiết của người nhà, tôi quyết định nhận điều trị bệnh nhân với hy vọng là làm được một điều gì đó cho người bệnh .Khám lâm sàng(18/10):
1.Khám lâm sàng:
1.1 Tổng quát: Chưa phát hiện bất thường.
1.2 Khám thần kinh:
Bệnh tỉnh tiếp xúc tốt, định hướng chính xác. 12 thần kinh sọ : bình thường.
Cảm giác nông: dị cảm kiến bò bàn tay và cẳng bàn chân 2 bên: bên (P) nặng hơn (T). Cảm giác sâu: cảm giác rung âm thoa có giảm ở ½ người (P) so với (T); định vị tư thế ngón bình thường.
Cơ lực: gốc chi và ngọn chân bên (P): 3/5, bên (T): 4/5, tay (P):1/5, tay (T): 2/5
Mất toàn bộ phản xạ gân cơ 4 chi. Teo cơ ngọn chi nhẹ, không có teo cơ khu trú, phản xạ riêng cơ (-).
2. Cận lâm sàng( kết quả bệnh nhân có từ 27/7 đến hiện tại):
-Huyết học: CTM 22 thông số: bình thường
-Sinh hóa: chức năng thận(BUN,Creatinin), gan(AST,ALT,GGT), bộ mỡ, Ion đồ: bình thường
-Miễn dịch học(sau ngày 18/10): HbsAg(+), AntiHBs (-), AntiHCV(-), HbeAg(-), AntiHBe(-), HIV(-)
-Hình ảnh học:
Siêu âm bụng tổng quát, siêu âm tim, doppler động mạch cảnh: bình thường
CTscan sọ não(27/7) MRI sọ não(30/9): bình thường
MRI cột sống cổ và thắt lưng( 29/9): bình thường
-EMG:
Tóm tắt kết quả EMG lần 2( 18/10):
*Điện cơ dẫn truyền:
–Dẫn truyền vận động: giảm, có hiện tượng hủy myelin và blốc dẫn truyền
-Dẫn truyền cảm giác: giảm, có hiện tượng blốc dẫn truyền
-Sóng F: giảm ở tay (T) và mất ở 3 chi còn lại.
*Điện cơ kim: -Có hiện tượng mất phân bố thần kinh ở các cơ ngọn chi khảo sát và phụ thuộc độ dài.
Kết quả EMG cho thấy:
1) Có hiện tượng hủy myelin dây thần kinh vận động và cảm giác ( thời gian tiềm dài, giảm tốc độ dẫn truyền và blốc dẫn truyền) ở các thần kinh khảo sát được.
2) Biểu hiện điện cơ dẫn truyền và điện cơ kim không đối xứng: bên (P) nặng hơn bên (T).
3) Giảm tần suất sóng F ở tay (P).
4) Mất toàn bộ dẫn truyền vận động ở 2 chân và tay (P).
5) Có hiện tượng hủy sợi trục thứ phát không đối xứng ở các cơ ngọn chi khảo sát: bên (P) nặng hơn (T), và phụ thuộc độ dài (chi dưới nặng hơn chi trên, gốc chi trên bình thường).
Vì bệnh diễn tiến nặng dần qua hơn 3 tháng, lâm sàng không đối xứng và đặc điểm điện cơ như mô tả ở trên nên bệnh nhân đã được chẩn đoán là EMG phù hợp biến thể CIDP: hội chứng Lewis-Sumner( MADSAM) có tổn thương sợi trục nặng hơn là hội chứng Lewis-Sumner( MADSAM) kinh điển.
Các vấn đề đặt ra trên bệnh nhân này là:
1)Vì sao bệnh nhân chẩn đoán sai
2) Điều trị bệnh nhân bị hội chứng Lewis-Sumner có kèm bệnh cảnh nền là nhiễm VGSV B mạn thì như thế nào?
- III. BÀN LUẬN
- Vì sao bệnh nhân chẩn đoán sai
Theo tôi là do :
- Triệu chứng yếu ½ người gặp ở tuyệt đại đa số bệnh nhân TBMMN. Theo Leger trong TKNB thì chỉ duy nhất ở bệnh nhân bị hội chứng Lewis-Sumner- một bệnh hiếm gặp của chuyên ngành thần kinh ngoại biên- là có biểu hiện này. Có rất nhiều bác sĩ chuyên khoa thần kinh không biết bệnh này do bệnh hiếm gặp, mới phát hiện từ 1982 và y văn đề cập rất ít.
- Số lượng bệnh nhân đến khám ngoại chẩn bệnh viện công lập nổi tiếng như bệnh viện 115, Chợ Rẫy,… thường quá tải, đặc biệt là trong những ngày đầu tuần, cho nên thời gian thăm khám bệnh trong lần khám đầu tiên ít. ( Trung bình 2-5phút/ bệnh nhân). Vì vậy để giải quyết áp lực quá tải của bệnh nhân, người bác sĩ thường chỉ là hỏi bệnh sử ngắn gọn và chỉ định cận lâm sàng ngay mà không đủ thời gian thăm khám tỉ mỉ các dấu chứng thần kinh ngoại biên như bệnh nhân nội trú.
- Trình độ dân trí hạn chế, kinh tế khó khăn: bệnh nhân thường rất chú trọng đến triệu chứng yếu liệt vận động vì sợ nguy hiểm đến tính mạng mà bỏ sót các triệu chứng cảm giác chủ quan.
Thế nhưng khi biểu hiện lâm sàng bệnh vẫn tiếp tục nặng dần lên trong 2 tháng trong khi hình ảnh CT scan sọ não và các xét nghiệm thường quy ban đầu hoàn toàn bình thường, thì chúng ta nên khám kỹ , xem xét lại chẩn đoán và nên làm thêm các xét nghiệm giúp củng cố hoặc loại bỏ chẩn đoán TBMMN.
- Điều trị cụ thể trên bệnh nhân:
Cho đến thời điểm hiện nay việc điều trị Hội chứng Lewis-Sumner dựa vào: IVIg( là lựa chọn đầu tiên) Corticoide( lựa chọn thứ 2), thay huyết tương( lựa chọn thứ 3), thuốc ức chế miễn dịch: Azathioprin, Cyclophosphamide,…Vì bệnh nhân bị nhiễm VGSV B nên đã được khuyến cáo điều trị ban đầu với truyền IVIg, nhưng do bệnh nhân không đủ điều kiện vì hoàn cảnh kinh tế khó khăn và không có BHYT.
Vì vậy tôi quyết định điều trị với Corticoide và vitamin B đồng thời theo dõi sát AST, ALT, GGT mỗi tuần và nếu cần làm xét nghiệm HBV-DNA định lượng, sau khi đã giải thích cặn kẽ các tác dụng phụ của Corticoids có thể gặp, đặc biệt là nguy cơ bùng phát VGSV B cho bệnh nhân và gia đình.
Đợt 1(18/10-15/11): Bệnh nhân được điều trị với Medrol 16mg: 4,5v/ngày( liều 1mg/kg/ ngày) + Neurobion: 2v/ngày, Nucleofort CMP: 2v/ngày và Omeprazol 20mg( Pháp): 1v/ngày trước ăn sáng 30ph. Xét nghiệm chức năng gan: AST:113U/l,ALT: 86U/l,GGT: 29U/l
Bắt đầu từ tuần 2 bệnh nhân bắt đầu có dấu hiệu cải thiện: cơ lực không yếu thêm và dị cảm không tăng thêm. Sau 3 tuần điều trị bệnh nhân hồi phục rõ rệt trên lâm sàng( cảm giác khỏe, cơ lực hồi phục, giảm dị cảm, ăn ngủ được) và kết quả EMG cải thiện rõ rệt(15/11). Tuy nhiên thế nhưng trên lâm sàng bệnh nhân bắt đầu có biểu hiện tác dụng phụ do dùng Corticoid: viêm dạ dày, hội chứng Cushing. Đặc biệt là xét nghiệm cho thấy tăng men gan( AST,ALT) nghi ngờ viêm gan siêu vi B tái hoạt động.
Vì vậy tôi đã cho làm xét nghiệm HBV-DNA định lượng lần 1(11/11/2014), kết quả 375.100IU/ml,
Đợt 2( 16/11-16/1/2015) Bệnh nhân được điều trị với Medrol 3,5v/ ngày + Neurobion: 2v/ngày, Nucleofort CMP: 2v/ngày + Fortec 25mg: 3v/ ngày+Morecal và Kaleorid 600mg: 1v/ ngày và Nexium 40mg: 2v/ ngày. Xét nghiệm chức năng gan bình thường: AST:25U/l,ALT: 20U/l,GGT: 23U/l. Bệnh nhân hồi phục rõ rệt trên lâm sàng( cơ lực hồi phục: sức cơ chân(P): 4/5,chân (T): 4-5/5, , tay (P):2/5, tay (T): 3/5 , hết dị cảm tê rần như kiến bò, phản xạ cơ tam đầu (+), ăn ngủ được).
Đợt 3( 17/1-4/2/2015) Bệnh nhân được điều trị với Medrol 2,5v/ ngày + Neurobion: 2v/ngày, Nucleofort CMP: 2v/ngày + Fortec 25mg: 3v/ ngày+Morecal và Kaleorid 600mg: 1v/ ngày và Nexium 40mg: 2v/ ngày. Bệnh nhân không có biểu hiện hồi phục thêm trên lâm sàng và bệnh nhân có dấu hiệu của viêm gan siêu vi B tái hoạt động với biểu hiện lâm sàng là chán ăn, đảo ngược khẩu vị và xét nghiệm cho thấy tăng men gan( AST: 98U/l,ALT: 211U/l). Vì vậy tôi đã cho làm xét nghiệm HBV-DNA định lượng lần 2(5/2/2015), kết quả: 35.617.650IU/ml.
Đợt 4( 5/2/2015-nay) Bệnh nhân được điều trị ngay với Tenofovir 300mg/ ngày + Neurobion: 2v/ngày, Nucleofort CMP: 2v/ngày + Fortec 25mg: 3v/ ngày+Morecal và Kaleorid 600mg: 1v/ ngày và Nexium 40mg: 2v/ ngày. Ngưng dùng Corticoids. Kết quả EMG (14/2): hồi phục thêm và khi làm điện cơ kim bệnh nhân biết đau.
Bệnh nhân không có biểu hiện hồi phục thêm trên lâm sàng và tình trạng viêm gan siêu vi B tái hoạt động đã được khống chế: với biểu hiện lâm sàng là thèm ăn trở lại và xét nghiệm cho thấy men gan về bình thường ( AST: 58U/l,ALT: 38U/l), xét nghiệm HBV-DNA định lượng lần 3(5/2/2015), kết quả: 41.690IU/ml. Việc điều trị Corticoids trở lại chỉ được xem xét với các điều kiện sau:
-Hoặc tình trạng viêm gan siêu vi B tái hoạt được kiểm soát(HBV-DNA định lượng tiếp tục giảm, men gan AST không tăng) và lâm sàng ,EMG ổn định sau 6 tháng.
-Hoặc lâm sàng , EMG có biểu hiện nặng lên
- Tham khảo y văn
Vào năm 1982 Lewis và cộng sự lần đầu tiên phát hiện trong số 40 bệnh nhân CIDP có 5 người bị bệnh dây thần kinh vận động cảm giác không đối xứng hầu hết ở chi trên với biểu hiện đa ổ ở nhiều dây thần kinh ngoại biên. Các ca bệnh này có biểu biện blốc dẫn truyền vận động đa ổ.
Vài năm sau(1988) Parry và Clarke cũng báo cáo 5 trường hợp bệnh có biểu hiện lâm sàng và điện cơ tương tự như Lewis và cộng sự.
Cho đến năm 2000 dã có 50 trường hợp hội chứng Lewis-Sumner(LSS) được báo cáo với nhiều tên gọi khác nhau về bệnh này: CIDP đa ổ ưu thế chi trên( upper limb predominant multifocal CIDP (Thomas et al., 1996; Gorson et al., 1999;Misra and Walker, 2000), bệnh dây thần kinh đa ổ có blốc dẫn truyền mãn tính( chronic multifocal neuropathy with persistent conduction block (Gibbels et al., 1993), bệnh dây thần kinh hủy myelin đa ổ đáp ứng Corticoid(steroid responsive multifocal demyelinating neuropathy (Liguori et al., 1999), bệnh dây thần kinh hủy myelin đa ổ do viêm (multifocal inflammatory demyelinating neuropathy (Van den Berg-Vos et al., 2000), bệnh dây thần kinh vận động và cảm giác hủy myelin đa ổ mắc phải (multifocal acquired demyelinating sensory and motor neuropathy (Saperstein et al., 1999), và bệnh nhiều dây thần kinh hủy myelin vận động và cảm giác ( motor and sensory demyelinating mononeuropathy multiplex (Oh et al., 1997). Điều này cho thấy sự khó khăn trong việc phân định vị trí của hội chứng Lewis-Sumner trong nhóm bệnh dây thần kinh do rối loạn miễn dịch( dysimmune neuropathies). Lúc bấy giờ bệnh này được cho là biến thể ít gặp của CIDP trong đó sự hủy myelin chỉ tập trung ở các thần kinh vận động. Về sau sự mô tả nhiều trường hợp tương tự và sự khác biệt trong đáp ứng điều trị so với CIDP,MMN nên bệnh này mới được công nhận như là 1 bệnh riêng biệt .
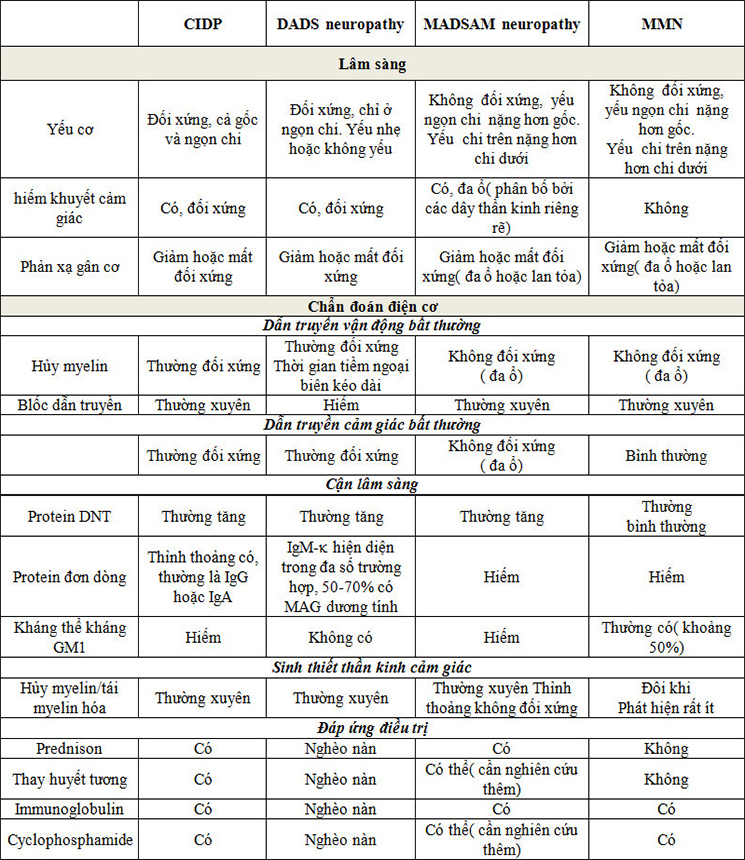
Cho đến hôm nay hầu hết các nhà thần kinh ngoại biên hàng đầu trên thế giới đều dựa vào bảng phân biệt của Sapentein và cộng sự (2001) các bệnh dây thần kinh hủy Myelin trung gian miễn dịch mắc phải mạn tính bao gồm:
1) Bệnh đa dây thần kinh hủy myelin do viêm mạn tính( chronic inflammatory demyelinating polyneuropathy: CIDP) là bệnh dây thần kinh gây yếu gốc và ngọn chi, đa số đối xứng và chủ yếu vận động.
2) Bệnh dây thần kinh vận động đa ổ( Multifocal motor neuropathy: MMN): với blốc dẫn truyền.
3) Bệnh dây thần kinh vận động và cảm giác hủy myelin mắc phải chủ yếu ở ngọn chi(Distal acquired demyelinating sensory and motor neuropathy : DADS)
4) Bệnh dây thần kinh vận động và cảm giác đa ổ, hay còn gọi là bệnh dây thần kinh vận động và cảm giác hủy myelin đa ổ mắc phải(multifocal acquired demyelinating sensory and motor neuropathy: MADSAM, hay còn gọi là hội chứng Lewis-Sumner: LSS).
Theo K. Viala và cộng sự( 2004) thì trong 23 trường hợp MADSAM( 17 nam và 6 nữ, được phát hiện và theo dõi trung bình 4 năm trong khoảng thời gian từ 11/1988-8/2002) thì:
1) Lâm sàng: có 16 bệnh nhân (70%) triệu chứng bắt đầu ở chi trên hầu hết liên quan đến thần kinh giữa hoặc trụ, 30% còn lại triệu chứng khởi đầu ở 1 chân với dị cảm ngọn chi và bàn chân rớt. Có 2 bệnh nhân biểu hiện yếu và teo cơ 4 đầu đùi và 1 bệnh nhân dị cảm ở vùng chi phối của thần kinh bì đùi ngoài. Triệu chứng khởi phát ở 1 bên là 17 bệnh nhân ( 74%), còn lại là 2 bên không đối xứng( 6 bệnh nhân, 26%). Có 5 bệnh nhân khởi phát 1 ổ liên quan đến thần kinh giữa, hoặc thần kinh trụ hoặc thần kinh quay hoặc thần kinh mác. Triệu chứng khởi phát vừa cảm giác và vận động là 15 bệnh nhân, còn lại là đơn thuần là cảm giác. Hầu hết triệu chứng cảm giác là tê bì và dị cảm, trong đó có 5 bệnh nhân biểu hiện đau nguồn gốc thần kinh.
2) Cận lâm sàng:
2.1 Dịch não tủy: Trong 18 bệnh nhân được chọc dò DNT thì có tăng nhẹ protein( 52-100mg/dl) gặp ở (6 bệnh nhân, 34%) , còn lại là bình thường.
2.2 Xét nghiệm đặc biệt:Kháng thể đơn dòng âm tính toàn bộ và 13/23 bệnh nhân được xét nghiệm kháng thể kháng GM1( IgM và IgG) đều âm tính.
2.3 Chẩn đoán điện cơ(EMG):
2.3.1 Dẫn truyền vận động
-100% bệnh nhân có blốc dẫn truyền ở chi trên, 4 bệnh nhân có blốc dẫn truyền ở chi dưới.
-83% bệnh nhân có giảm tốc độ dẫn truyền vận động và sóng F bất thường( thời gian tiềm sóng F kéo dài hoặc mất sóng F) ở ít nhất 1 dây thần kinh.
2.3.2 Dẫn truyền cảm giác: Biên độ dẫn truyền cảm giác(SNAP) ngoại biên giảm ở 20 bệnh nhân(87%), blốc dẫn truyền cảm giác gặp ở 57%.
2.3.3 Điện cơ kim: có hiện tượng mất phân bố thần kinh ở các cơ ngoại biên gặp ở 6 bệnh nhân.
2.3.4 Điện thế gợi cảm giác thân thể(SEP): có 1 bệnh nhân bất thường.
3) Điều trị:
Theo y văn thì việc sử dụng Corticoids trong điều trị hội chứng Lewis-Sumner bằng đường uống chỉ có hiệu quả rõ rệt trong 33% trường hợp(K. Viala và cộng sự, 2004), 3/14 trường hợp (Zachary Simmons, 2011) 25% (Shahram Attarian và cộng sự, 2011). Hiện nay trong y văn chưa có trường hợp nào ghi nhận dùng Corticoid trên bệnh nhân bị hội chứng Lewis-Sumner có nhiễm VGSV B mạn tính.
Thế nhưng trong điều kiện bệnh nhân nghèo ở Việt Nam thì hầu như không có cách điều trị nào khác. Theo y văn từ chuyên ngành tiêu hóa gan mật thì :
+ Có 20-50% bệnh nhân bị viêm gan siêu vi B mãn hoặc người lành nhiễm VGSV B sẽ tái hoạt động khi dùng các thuốc ức chế miễn dịch hoặc dùng Corticoide.
+ Việc dùng Corticoide chỉ an toàn cho các đối tượng này nếu liều dùng <20mg/ngày kéo dài. Bệnh nhân được xem là có nguy cơ cao của tái hoạt hóa VGSV B khi dùng Corticoids ≥ 20mg/ ngày trong ít nhất 4 tuần.
+ Bằng chứng VGSV B tái hoạt động biểu hiện khi: hoặc HBV-DNA(+) khi trước đó âm tính hoặc HBV-DNA> 2 log10 IU/mL ở bệnh nhân có HBV-DNA(+) ở mức ban đầu( baseline) ( vài y văn: tăng > 10 lần so với mức ban đầu).
+ Yếu tố quan trọng nhất của tái hoạt hóa VGSV B là định lượng HBV-DNA> 105 copies/mL (khoảng 104 IU/mL).
+ Nếu có bằng chứng của VGSV tái hoạt hóa thì sử dụng ngay Entecavir hoặc Tenofovir điều trị. Không dùng Tenofovir khi có suy giảm chức năng thận.
+ Điều trị thuốc kháng vi rus ít nhất 6 tháng sau khi ngưng sử dụng Corticoids.
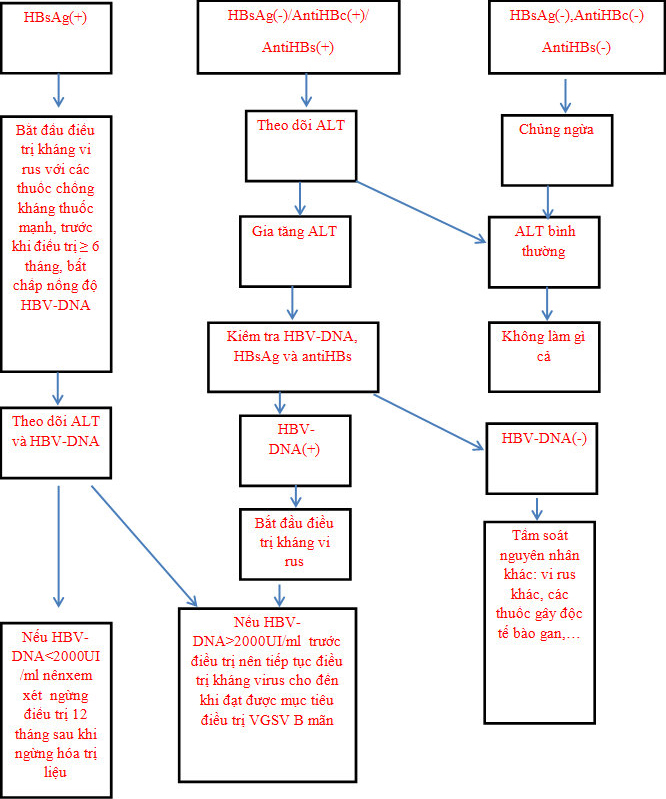
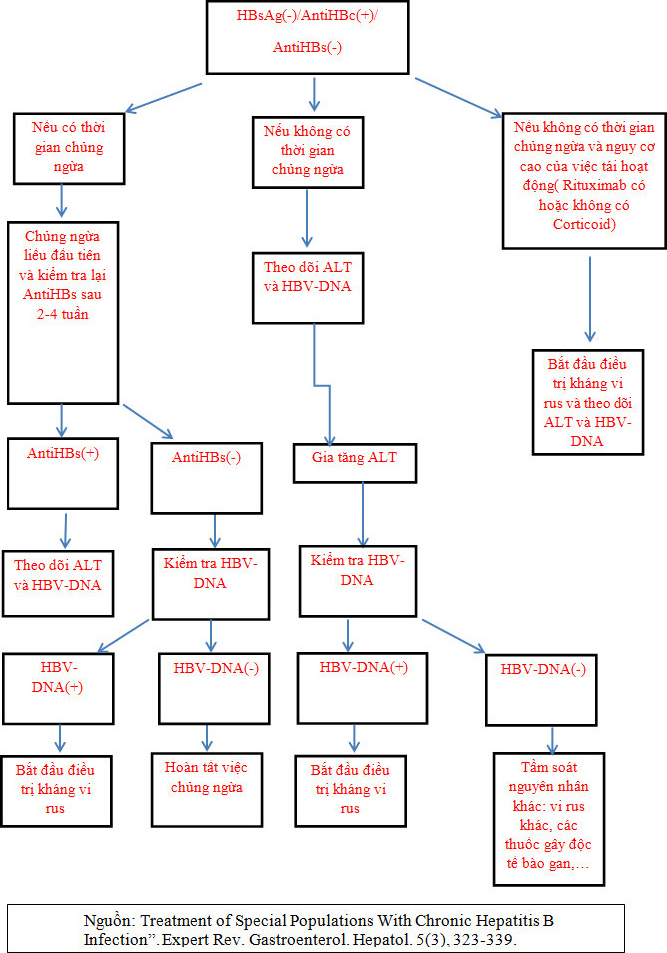
Sơ đồ theo dõi và điều trị bệnh nhân nhiễm VGSV B có nguy cơ cao suy giảm miễn dịch
Sơ đồ theo dõi và điều trị bệnh nhân nhiễm VGSV B có nguy cơ cao suy giảm miễn dịch
KẾT LUẬN
- Cần khám kỹ và xem xét lại chẩn đoán TMMMN khi lâm sàng biểu hiện nặng lên và hình ảnh học không tương thích. Các biểu hiện lâm sàng không đối xứng đặc biệt là rối loạn cảm giác, phản xạ gân cơ,…có thể gợi ý đến hội chứng Lewis-Sumner.
- Tham khảo ý kiến các đồng nghiệp chuyên ngành khác là quan trọng.
TÀI LIỆU THAM KHẢO
1) Shahram Attarian, Annie Verschueren, Je´ Rome Franques( 2011). “Response to treatment in patients with lewis–sumner syndrome”. Muscle Nerve 44: 179–184.
2) Antonios Bayas , Ralf Gold , Markus Naumann(2013).” Long-term treatment of Lewis–Sumner syndrome with subcutaneous immunoglobulin infusions”. Journal of the Neurological Sciences Volume 324, Issues 1-2, pp 53–56. Available from: http://dx.doi.org/10.1016/j.jns.2012.09.033
3) Pierre R. Bourque, JodiWarman Chardon, RamiMassie(2015).” Autoimmune peripheral neuropathies” Clin Chim Acta (2015), Available from: http://dx.doi.org/10.1016/j.cca.2015.02.039
4) Mazen M. Dimachkie, Richard J. Barohn, Jonathan Katz(2013)” Multifocal Motor Neuropathy,Multifocal Acquired Demyelinating Sensory and Motor
Neuropathy, and Other Chronic Acquired Demyelinating Polyneuropathy Variants”. Neurol Clin 3, pp 533–555. Available from: http://dx.doi.org/10.1016/j.ncl.2013.01.001.
5) Lawrence S Friedman(2015) Approach to the patient with abnormal liver biochemical and function tests. Available from: Uptodate.com.
6) Praful Kelkar, Suraj Ashok Muley(2006).” Chronic inflammatory demyelinating polyradiculoneuropathy and multifocal motor neuropathy”. In: J. Kimura (Ed.)Peripheral Nerve Diseases. Handbook of Clinical Neurophysiology, Vol. 7, pp 709-723.
7) Anna SF Lok, Peter A L Bonis(2015)”Hepatitis B virus reactivation associated with immunosuppressive therapy”. Available from: Uptodate.com.
8) Young-Eun Park, Ji-Won Yook,Dae-Seong Kim(2010)”A Case of Lewis-Sumner Syndrome Showing Dramatic Improvement after Plasma Exchange”. J Korean Med Sci; 25: 1101-1104.
9) Irene N. Rapti, Stephanos J. Hadziyannis, (2011) “Treatment of Special Populations With Chronic Hepatitis B Infection”.Expert Rev. Gastroenterol. Hepatol. 5(3), 323-339.
10) K. Viala, L. Renie, T. Maisonobe et al(2004) “Follow-up study and response to treatment in 23 patients with Lewis–Sumner syndrome”. Brain ; 127: 2010–2017
11) David s. Saperstein, Anthony A. Amato, Gil I. Wolfe et al(1999).” Multifocal acquired demyelinating sensory and motor neuropathy: the Lewis–Sumner syndrome”. Muscle Nerve 22: 560–566.
12) Zachary Simmons(2011),”Treatment and Management of Specific Neuromuscular Disorders” In: Tulio E. Bertorini(Ed.). Neuromuscular Disorders: Treatment and Management, Saunders , pp 215-235.